CEC2024 | 戴力教授团队:从左侧头臂静脉闭塞的治疗需求看静脉支架的设计创新


2024年10月31日—11月3日,备受瞩目的第十五届中国血管论坛(CEC2024)于北京盛大召开,国内外专家齐聚一堂共襄盛会。本次大会设置知名专家面对面、中青年专家论坛、学术专题讲座,病例直(录)播、外周血管介入前沿与争锋辩论赛、疑难病例大查房、复杂血管疾病、血管外科危重症管理、血管疾病治疗并发症处理及预防、外周器械新技术新疗法、下肢动脉减容规范化应用最新证据深度解读、国际专场@CEC等热点板块,全面展现最新的血管疾病诊疗方法和技术,为广大血管外科医务工作者及同道提供了一场内容丰富、高质量、高水平的学术盛宴。
本次大会期间,大连医科大学附属第二医院戴力教授团队为各位专家同道介绍了《从左侧头臂静脉闭塞的治疗需求看静脉支架的设计创新》。欢迎阅读。
演讲题目:
《从左侧头臂静脉闭塞的治疗需求
看静脉支架的设计创新》
演讲嘉宾:
戴力教授
单位:
大连医科大学附属第二医院

前言
左侧头臂静脉受压综合征是一种由周围复杂解剖结构压迫引起的静脉回流障碍性疾病。随着血液透析、心脏起搏器植入等医疗操作的增多,继发性中心静脉病变也日益常见。本文基于左侧头臂静脉独特的解剖环境及临床治疗挑战,分析了现有静脉支架的局限性,并探讨了面向未来的静脉支架设计创新方向,包括柔顺性、支撑力、贴壁性及精准定位等方面的优化。

左侧头臂静脉的独特解剖结构
与“四面楚歌”的受压境地
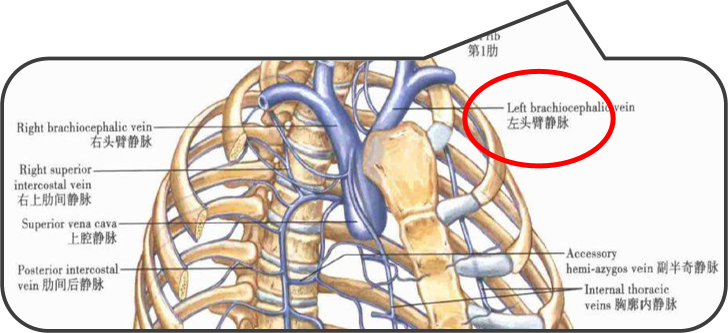
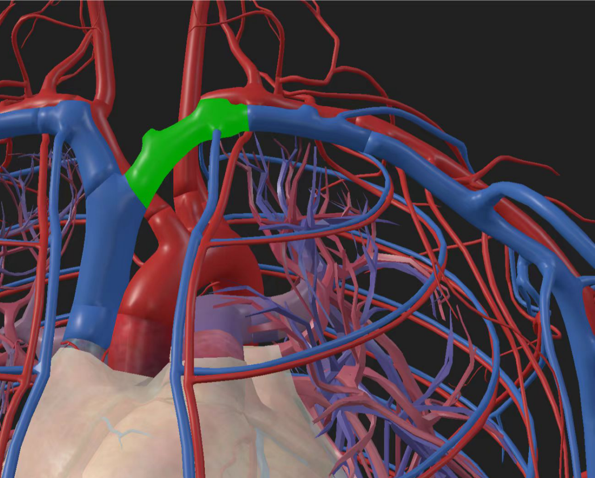
左侧头臂静脉(又称无名静脉)的走行路径决定了其易于受压的解剖学基础。它处于一个狭小的“解剖三角”内,可谓是“四面楚歌”:
后侧: 受到头臂干、左颈总动脉和左锁骨下动脉的压迫,更深层还有坚硬的气管进一步加强压迫。
下方: 随着主动脉弓的硬化扩张,会自下向上对静脉产生挤压。
前侧: 受到胸骨的限制。
此外,胸骨的正常变异也不容忽视。上胸骨小骨 是一种存在于约1.5%人群中的正常变异,在亚洲人群中发生率更高(约3.8%)。如图A(轴位视图)和图B(矢状位视图)所示,这些小骨位于胸骨柄后方,可能与胸骨柄完全分离,进一步增加了左头臂静脉前方受压的风险。
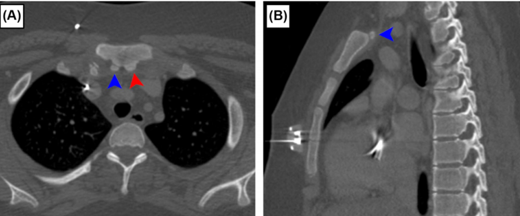
图A & 图B:上胸骨小骨(EO)的解剖位置
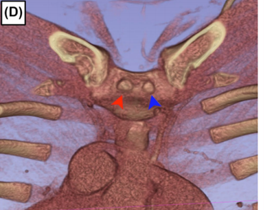
图D:左侧头臂静脉周围骨骼与软组织关系示意图(黄色:骨骼结构;红色:软组织)
这种多方向的持续性或间歇性压迫,是导致左侧头臂静脉压迫综合征(Innominate Vein Compression Syndrome, IVCS) 的根本原因。该综合征由A. Wurtz于1989年首次提出,也称为单侧上腔静脉综合征。

继发性中心静脉病变加剧治疗需求
除了原发性解剖压迫,医源性或治疗相关的中心静脉病变也日益成为临床挑战:
1
临床挑战
动静脉内瘘(AVF)相关狭窄/阻塞: AVF建立后,血流动力学发生剧变,高流速和湍流会增加对静脉壁的剪切力,导致内皮损伤、内膜增生和纤维化,最终引发狭窄或闭塞。
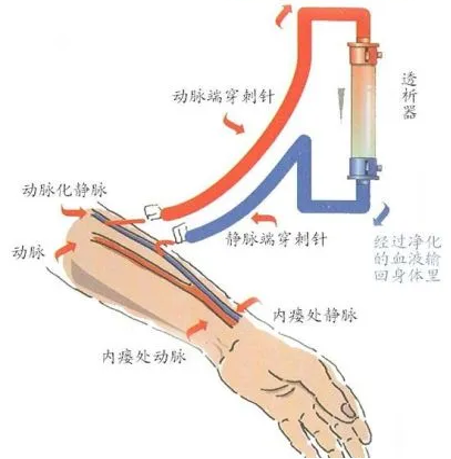
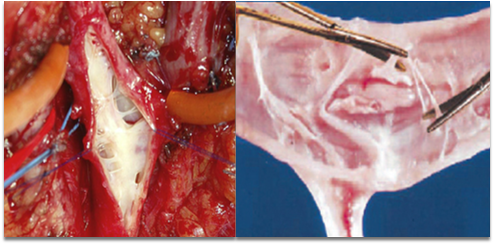
图:动静脉内瘘(AVF)相关狭窄/阻
导联相关性静脉狭窄/闭塞(LRVSO): 心脏起搏器、植入式心脏转复除颤器(ICD)等装置导联的植入,会引发内皮损伤、炎症反应和纤维蛋白沉积。随时间推移,导线周围会形成富含胶原的纤维鞘,甚至将多根导线捆绑在一起,导致静脉管腔狭窄或闭塞。
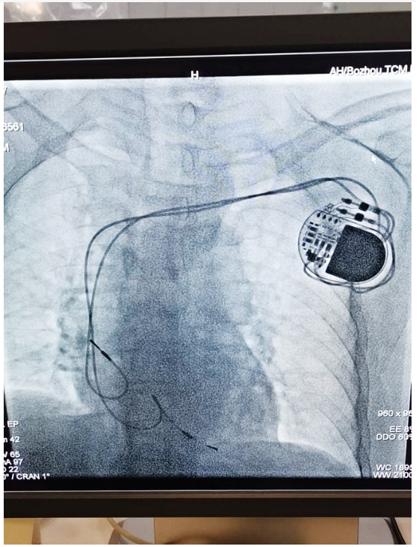
导管源性静脉狭窄/闭塞: 反复的中心静脉置管会引起静脉壁损伤,同样通过内膜增生机制导致狭窄。
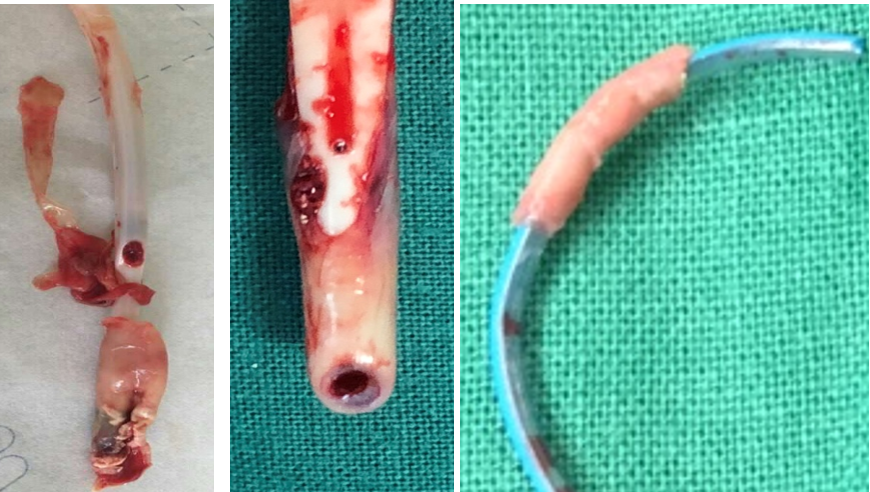
图:导管源性静脉狭窄/闭塞
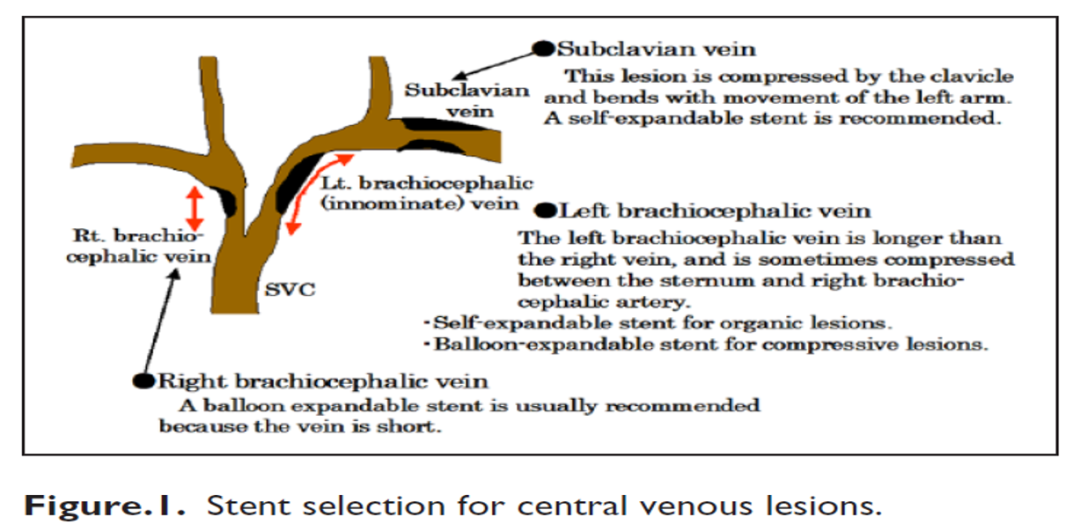
图:肾功能不全患者中心静脉狭窄或闭塞常见部位
2
病例展示
�� 病例一:
术前:患者表现为左侧手臂、颜面部肿胀,胸壁静脉怒张,AVF无法正常透析。
手术过程:造影证实为左侧头臂静脉闭塞。经球囊扩张成形术后,症状完全缓解,内瘘恢复正常使用。
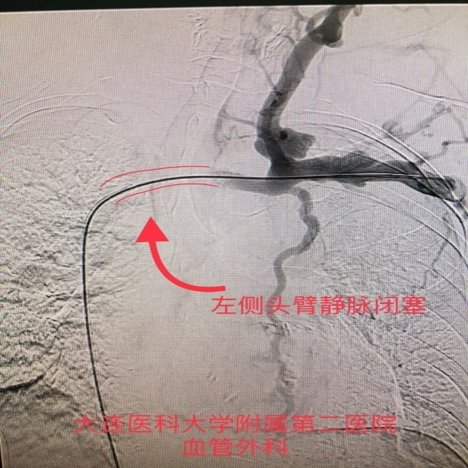
图:造影证实左侧头臂干静脉闭塞
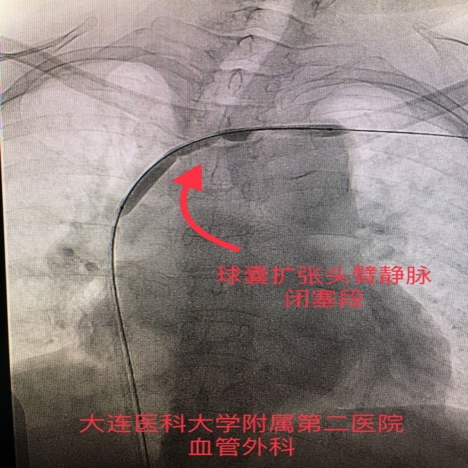
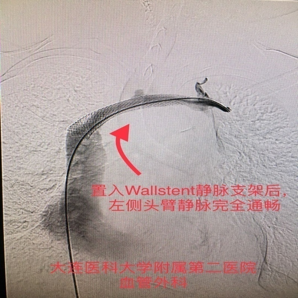
图:球囊扩张左侧头臂干静脉闭塞段
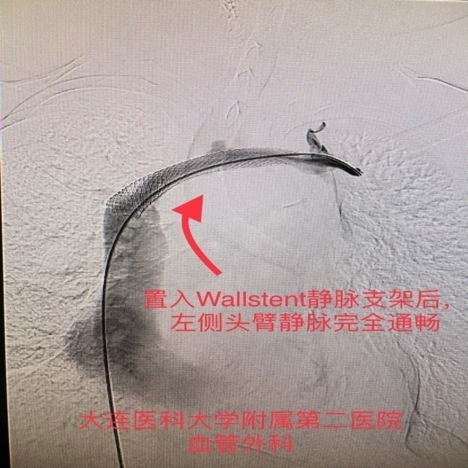
图:左侧头臂静脉完全通畅
术后:术后患者左上臂、左侧颜面部消肿,左侧胸壁曲张静脉消失,左侧动静脉内瘘正常使用。
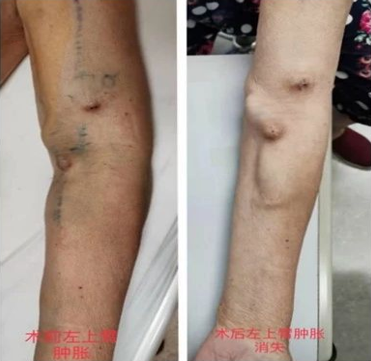
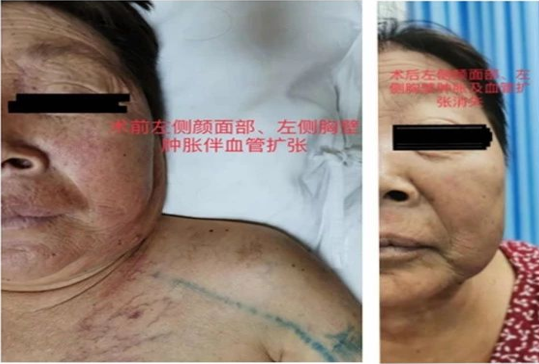
图:术后照片
�� 病例二:
术前造影


建立通道


球囊扩张、支架置入
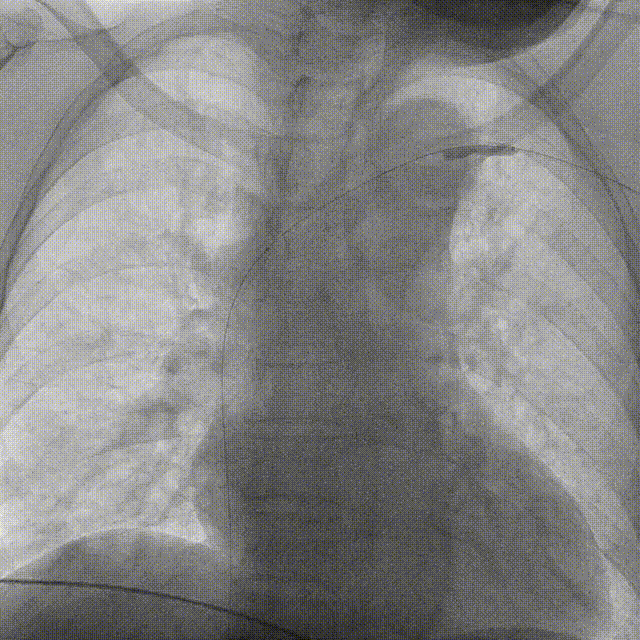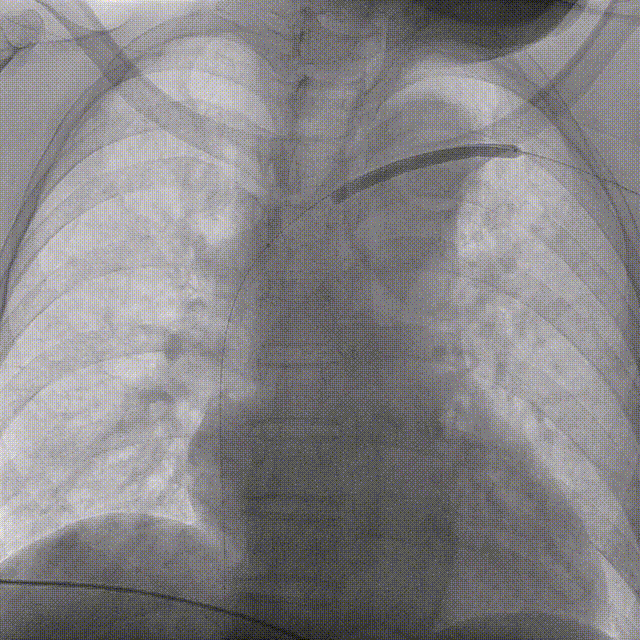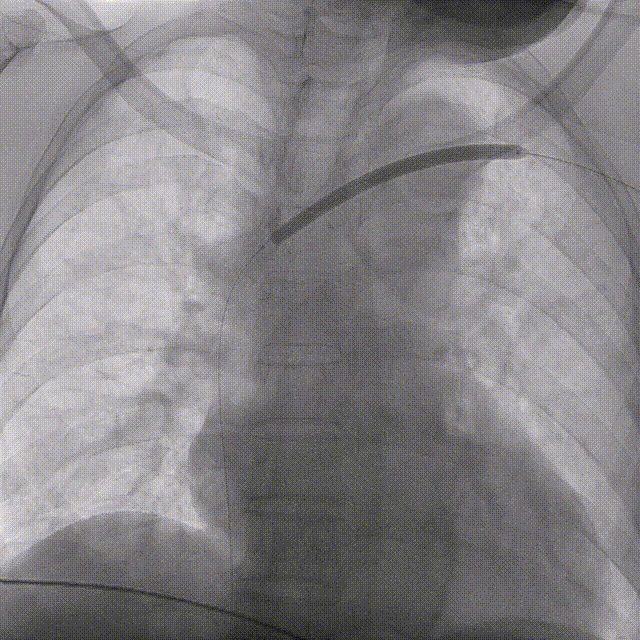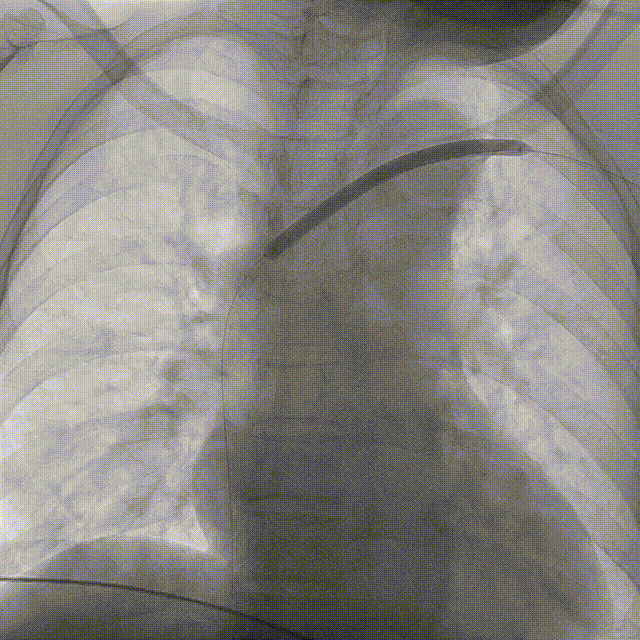

��病例三:
术中造影
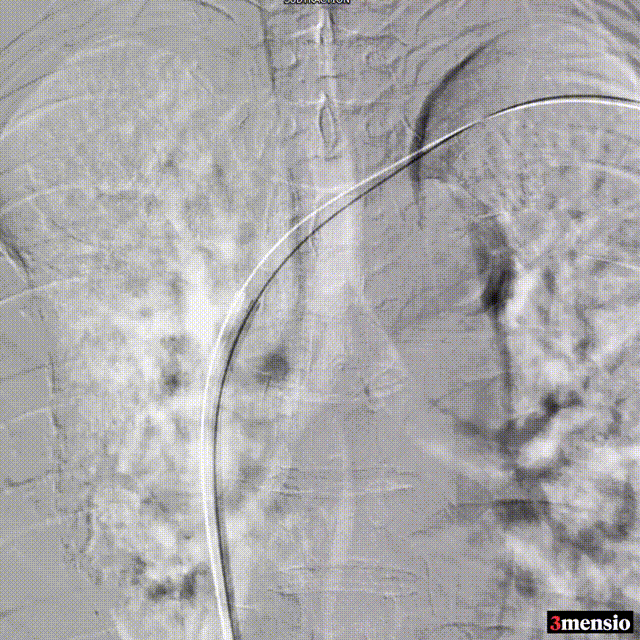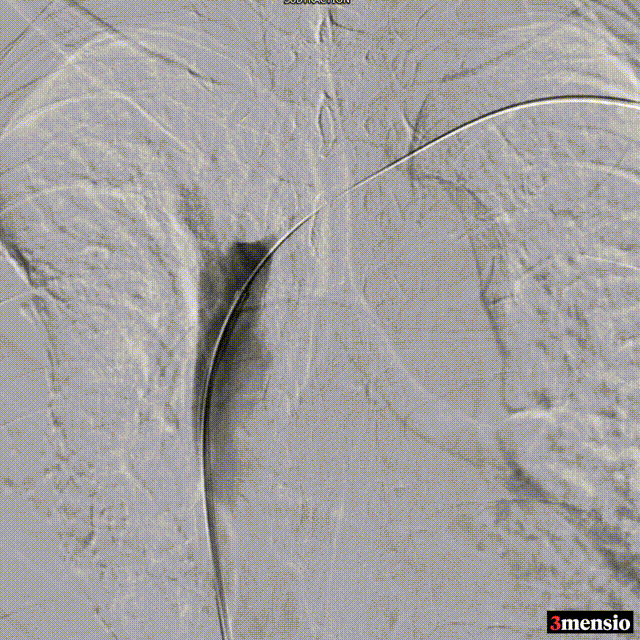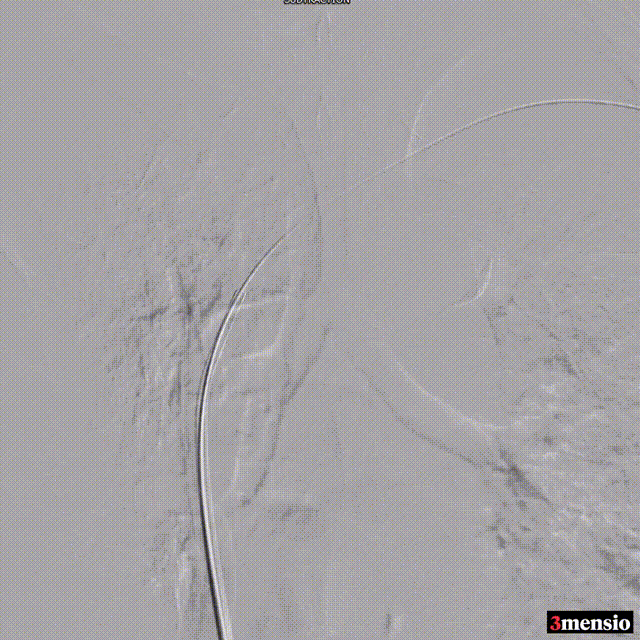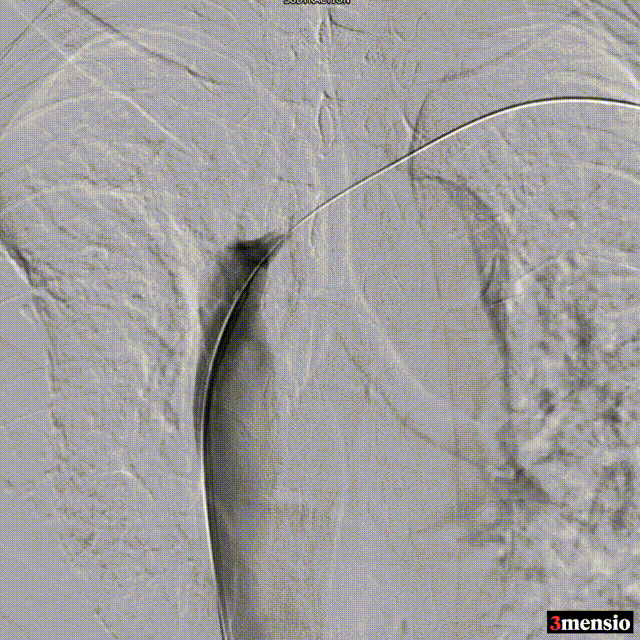

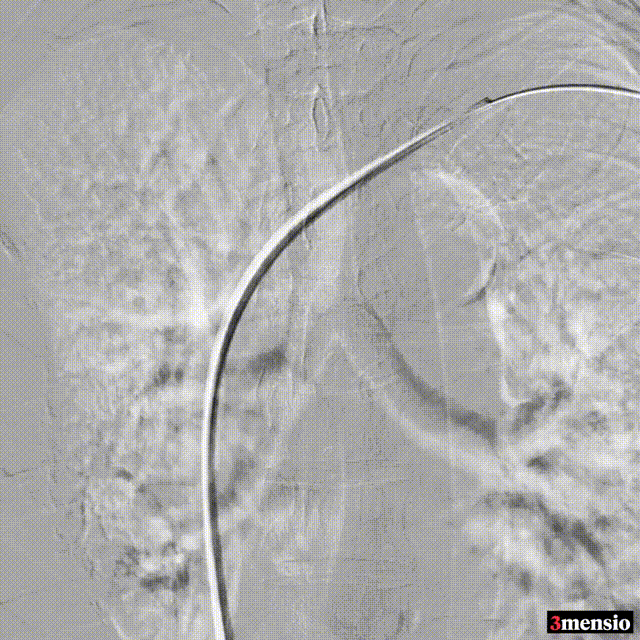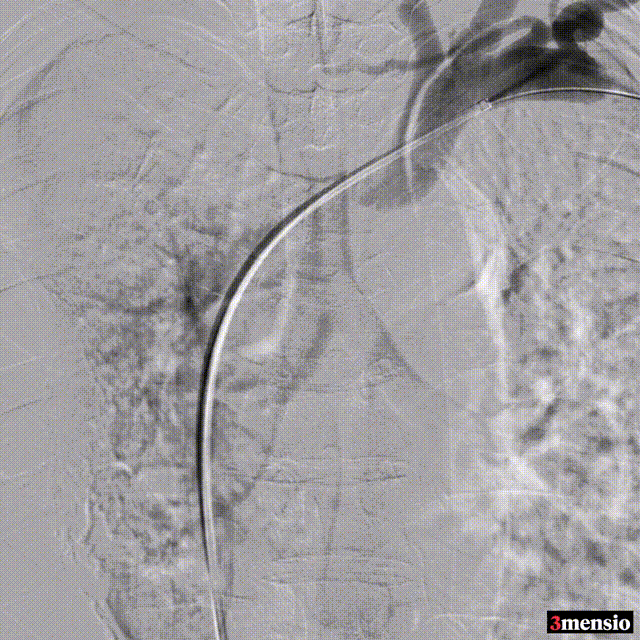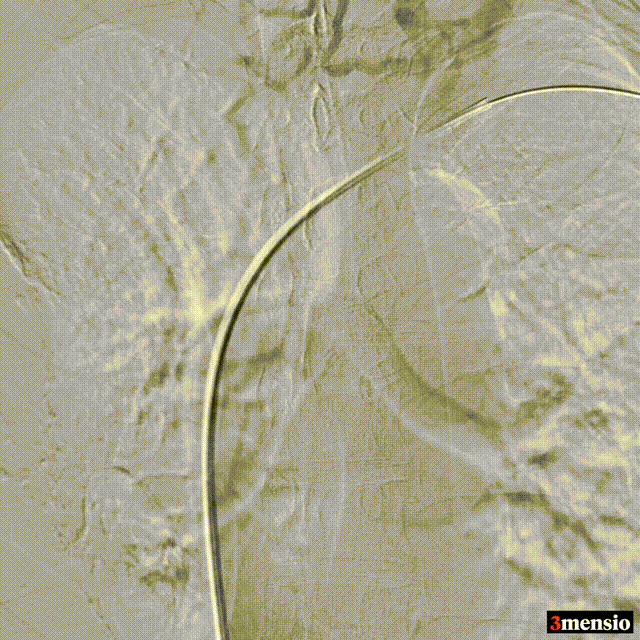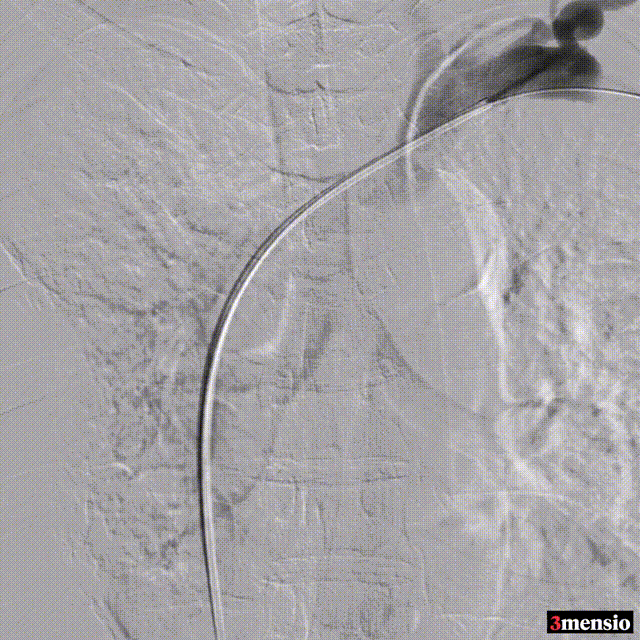
图:术中造影
术后:支架定位困难,未能完全覆盖病变
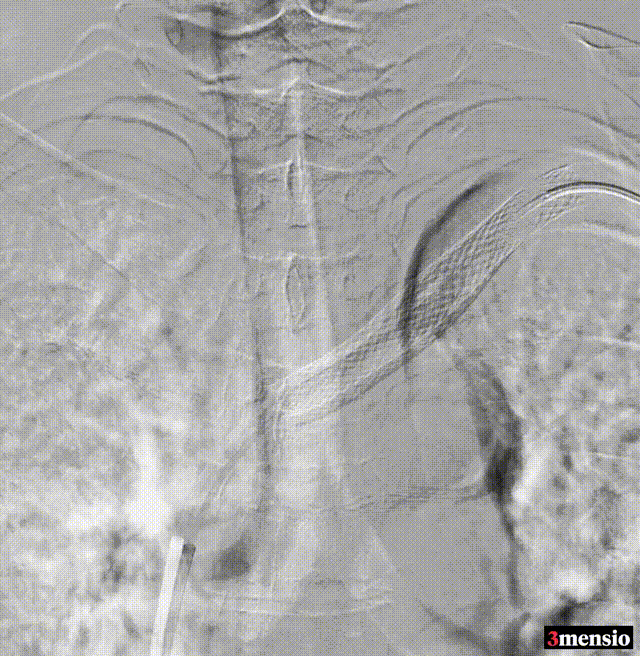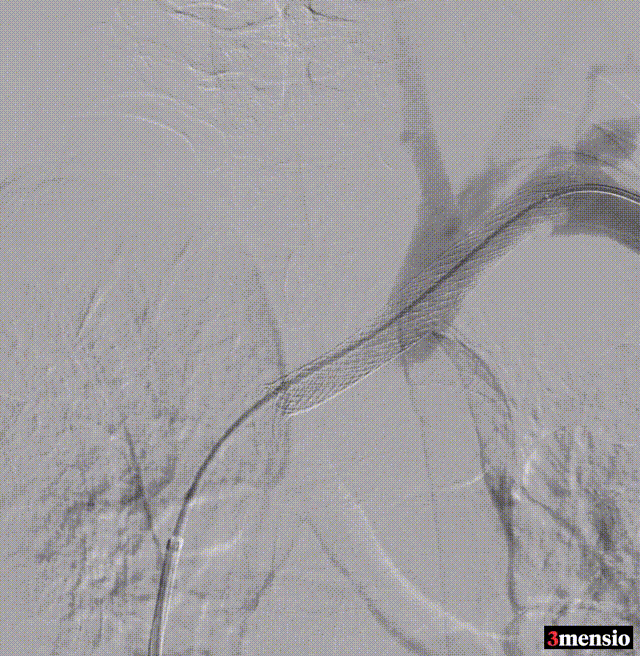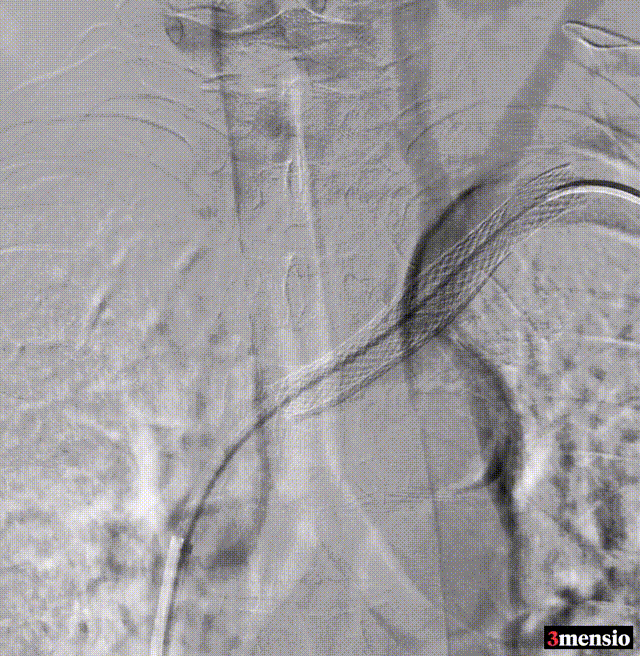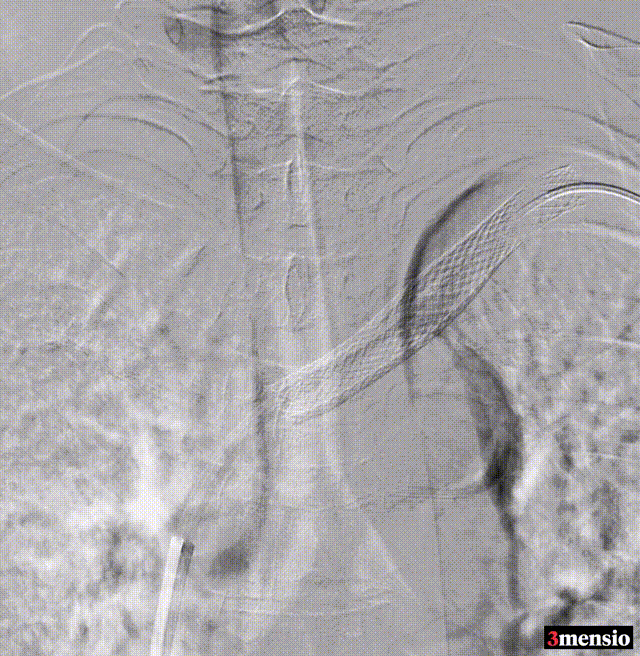
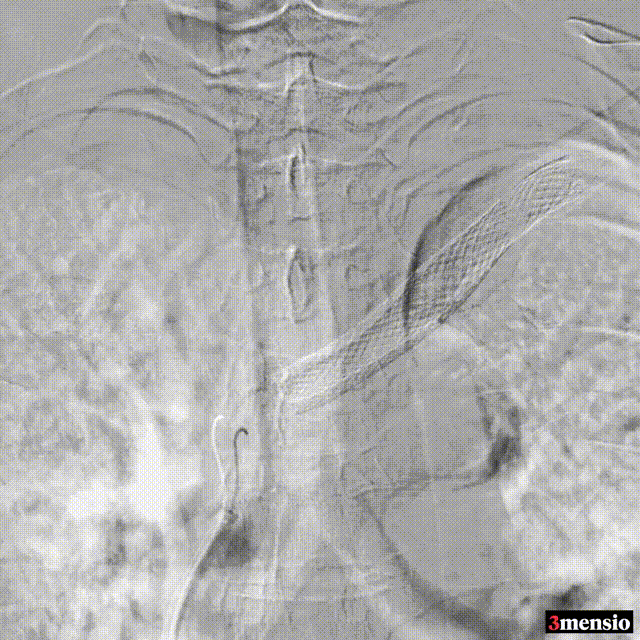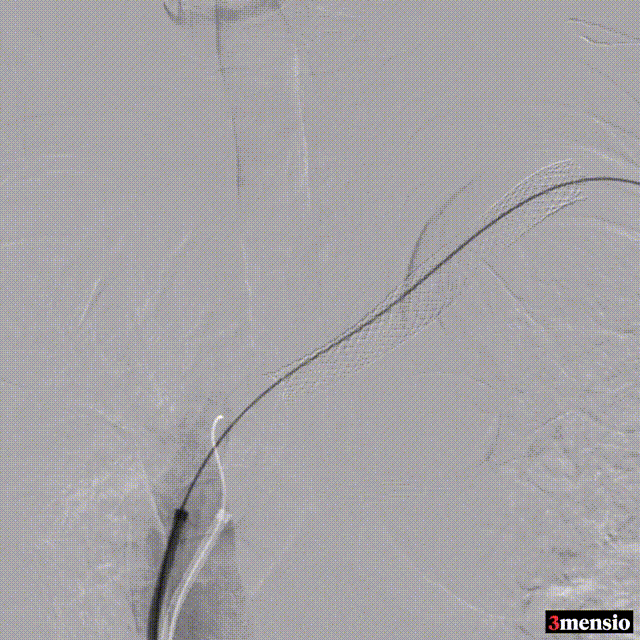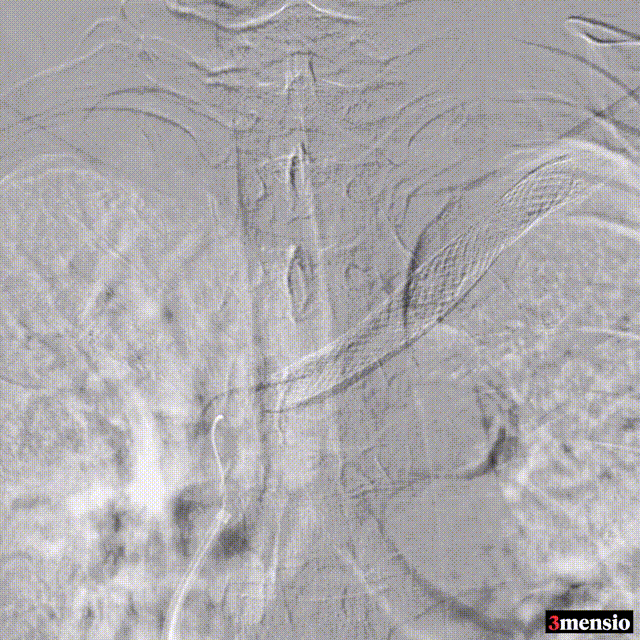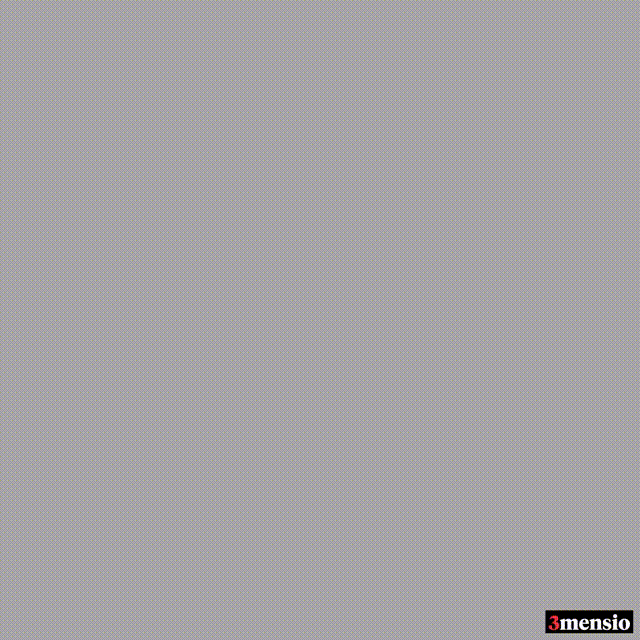
图:术后
�� 病例四:左头臂干静脉狭窄、闭塞
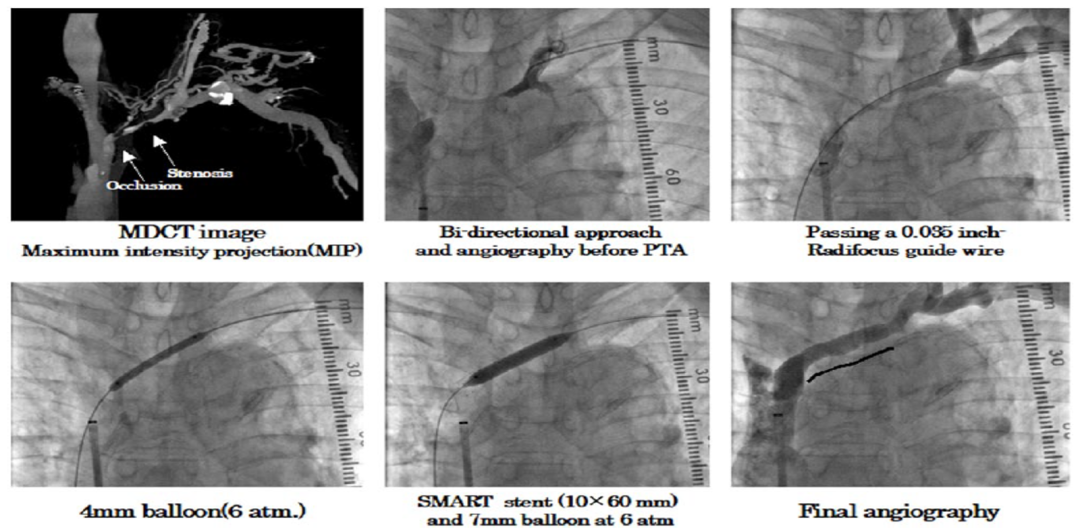
图:手术过程
�� 病例五:左侧头臂静脉狭窄
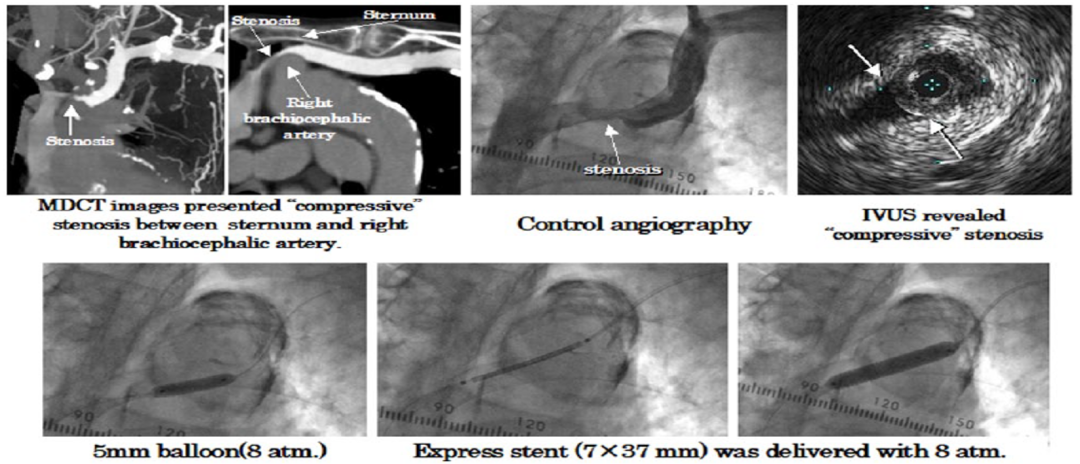
图:手术过程

现有静脉支架在治疗中面临的挑战
针对上述复杂的静脉病变环境,现有的静脉支架暴露出诸多不足:
★ 支撑力不足
对于May-Thurner综合征、IVCS等外部压迫性病变,若支架径向支撑力不足,无法有效抵抗外部压力,会导致支架塌陷和再狭窄。
★ 柔顺性差
难以适应静脉自然的弯曲形态,显得僵硬。
可能导致血管被强行拉直,引发不适或新的血流动力学问题。
在弯曲部位易发生弯折(Kink),造成管腔闭塞。
产生“竹节样效应(Bamboo stick effect)”,影响支架整体性能。
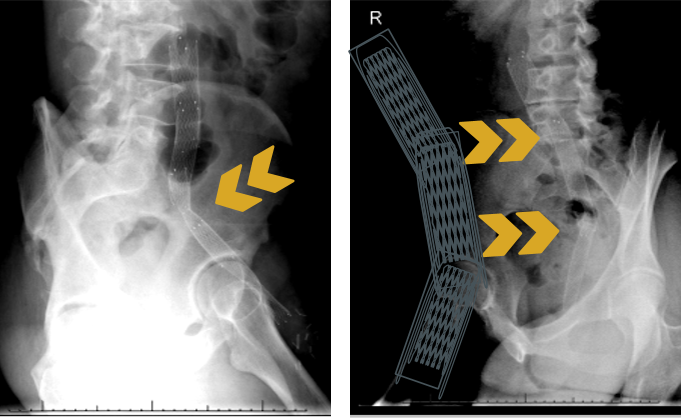
图:弯折 Kink
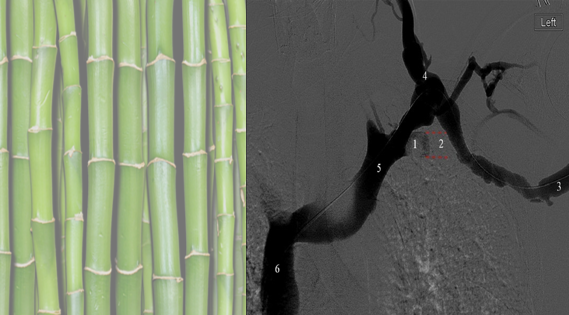
图:血管拉直
★ 贴壁性不良
支架与静脉壁之间若存在空隙,容易导致复发或新发血栓。无论是编制支架还是开环/闭环设计,贴壁性都是关键。
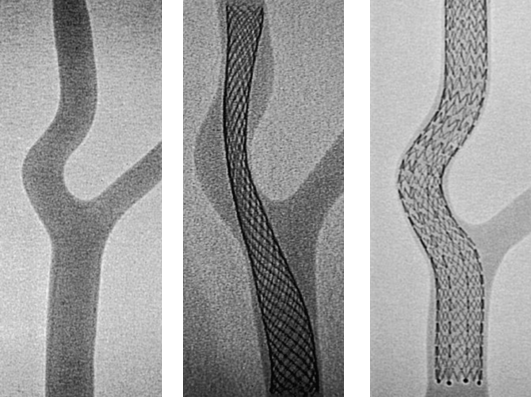
闭环支架
开环支架
图:贴壁良好
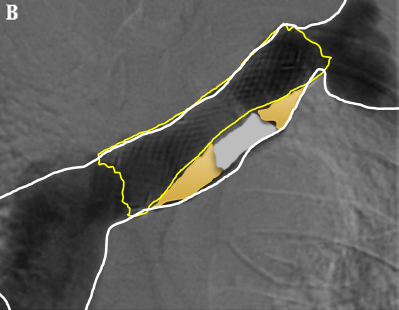
图:贴壁不良
★ 定位困难,长度不可控
释放过程中支架定位不精准,无法精确控制其突入上腔静脉或下腔静脉的长度,这是现有器材的局限性,可能导致并发症或影响未来治疗选项。



静脉支架的设计创新方向与研究基础
为解决上述挑战,静脉支架的设计需要多方面的创新。
01
支架形态与近端设计
对于静脉分叉口(如头臂静脉汇入上腔静脉处)的病变,支架近端的斜面设计 比平头设计更符合解剖生理,能减少对血流的影响和对对侧静脉开口的干扰。对于长度超过2cm的病变,可能需要特殊形态的支架来确保完全覆盖且不影响重要侧支。
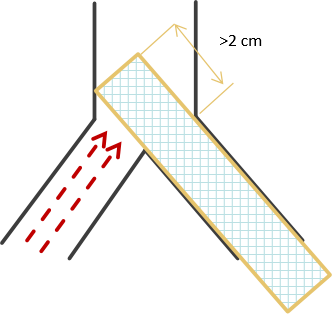

图:平头支架与斜面支架在静脉分叉处的效果对比
02
提升柔顺性结构研究与优化
通过建立支架柔顺性与结构参数(如连接单元、支撑单元的形状和分布)之间的数学模型,可以进行针对性的结构设计创新。研究通过模拟不同挠度(如0.5mm, 1.0mm, 2.0mm)下的形变,优化支架端部、主体结构和过渡部分的设计,从而显著提高其弯曲和扭转的顺应性。
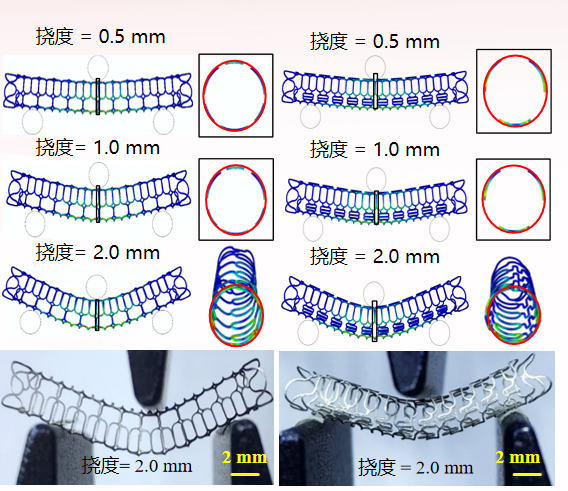
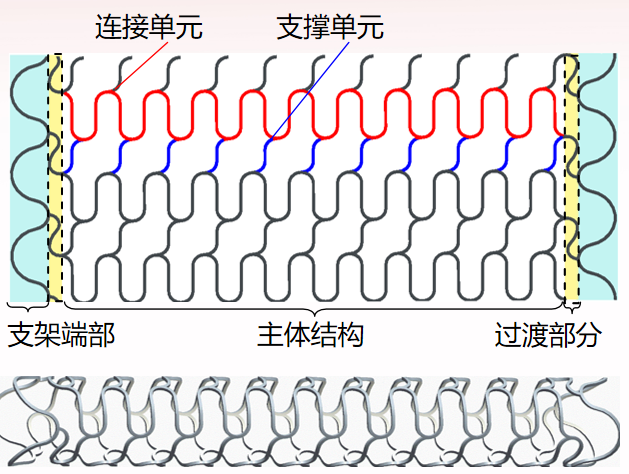
图:不同结构设计在相同挠度下的形变对比
03
多目标结构优化设计
利用先进的优化算法(如基于Kriging代理模型的优化设计流程)进行多目标优化,可以同时平衡支架的支撑力、柔顺性、贴壁性等性能。此方法已成功应用于:
结构优化: 消除支架扩张后的“狗骨头”效应(两端过度扩张),使血管内支撑更均匀。
药物释放优化: 改善载药支架的药物释放特性,实现更持久、有效的抗增生治疗。
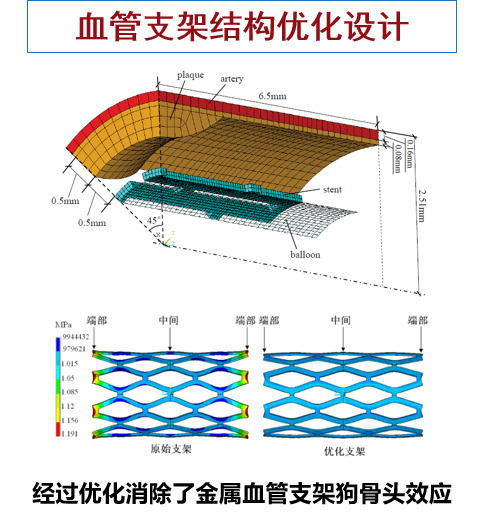
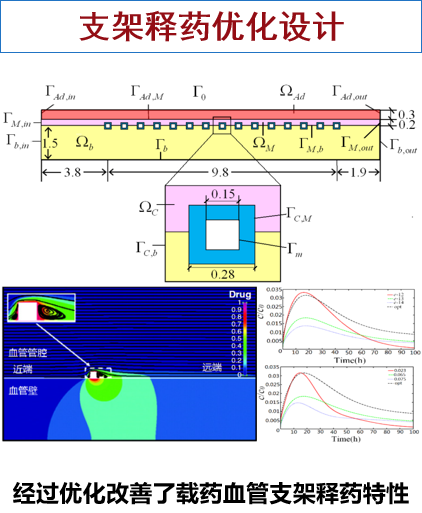
总结与展望:CAS的未来发展方向
左侧头臂静脉受压综合征及其相关中心静脉病变的治疗,对静脉支架的性能提出了极高要求。当前支架在支撑力、柔顺性、贴壁性和精准定位方面仍存在明显短板。未来的发展方向是依托先进的数学模型和多目标优化设计方法,开发出新一代的专用静脉支架。这种支架应能完美适应静脉独特的解剖和血流动力学环境,具备足够的支撑力以抵抗外部压迫,优异的柔顺性以顺应血管形态,良好的贴壁性以防止血栓形成,以及可控的释放精度以确保治疗效果。这将为众多患有复杂中心静脉疾病的患者带来更安全、更有效的治疗选择。
专家介绍

戴力教授
大连医科大学
附属第二医院
血管外科副主任
教授
中国医师协会血管外科医师分会腹主动脉学组委员 中国医师协会血管外科医师分会静脉血栓与肺栓塞学组委员
辽宁省医学会血管外科学分会委员会委员
中国研究型医院学会血管医学专业委员会全国委员
