CEC2024 | 戈小虎教授:B型夹层TEVAR后逆行性A型夹层的诊治体会

 16年来,一直陪伴中国血管医生成长
16年来,一直陪伴中国血管医生成长 

2024年10月31日—11月3日,备受瞩目的第十五届中国血管论坛(CEC2024)于北京盛大召开,国内外专家齐聚一堂共襄盛会。本次大会设置知名专家面对面、中青年专家论坛、学术专题讲座,病例直(录)播、外周血管介入前沿与争锋辩论赛、疑难病例大查房、复杂血管疾病、血管外科危重症管理、血管疾病治疗并发症处理及预防、外周器械新技术新疗法、下肢动脉减容规范化应用最新证据深度解读、国际专场@CEC等热点板块,全面展现最新的血管疾病诊疗方法和技术,为广大血管外科医务工作者及同道提供了一场内容丰富、高质量、高水平的学术盛宴。
本次大会期间,新疆自治区人民医院血管外科戈小虎教授与各位专家同道分享讨论了《B型夹层TEVAR后逆行性A型夹层的诊治体会》。欢迎观看。
演讲题目:
《B型夹层TEVAR后逆行性
A型夹层的诊治体会》
演讲嘉宾:
戈小虎教授
单位:
新疆自治区人民医院血管外科
前
言
逆行性A型夹层(retrograde type A dissection RTAD)是指在胸主动脉腔内修复术(TEVAR)后,主动脉夹层从降主动脉逆行扩展至升主动脉的灾难性并发症之一。根据不同研究,TEVAR术后RTAD的发生率为2%至8%,死亡率高达37.1%至42.2%。关于TEVAR术后RTAD发生的数据有限,本文详细归纳分析了RTAD的发生率、死亡率、危险因素、治疗策略和预防措施等方面,并结合作者所在中心的临床病例进行了深入讨论。
文献研究
发生率与死亡率
Yanqing Chen等(2017年)纳入50篇原始研究共8969例。汇总TEVAR术后RTAD的发生率为2.5%,相关病例的死亡率为37.1%。
Yammine H等(2019年)分析2012年1月至2017年1月收治的186例TEVAR的TBAD,共有15例出现RTAD,该研究队列中,RTAD发生率为8%。
Ali-Hasan-Al-Saegh等(2023年)10600名患者中有285人发生RTAD:估计RTAD发生率为2.3%,荟萃分析估计死亡率为42.2%。
Tao Ma等(2018年)纳入2005年4月-2013年10月单中心997例接受TEVAR治疗的TBAD患者,并对852例(83.28%)患者进行随访(0-6年;平均2.6年),RTAD发生率为3.17%(27例)。
发生率
总体发生率:Meta分析显示TEVAR术后RTAD发生率为2.3%-3.17%(Chen et al., 2017; Ali-Hasan-Al-Saegh et al., 2023),单中心研究可达8%(Yammine et al., 2019) 。
时间分布:急性B型夹层RTAD发生率是慢性的1.8倍,但部分病例可在术后1年甚至更晚发生(中位间隔时间4.6个月)。
死亡率
总体死亡率:约37.1%-42.2%,需外科干预的病例术后死亡率可降至13.6%。TEVAR后RTAD罕见,但死亡率高,特别是在TEVAR后的第一个月。
生存率:急诊手术生存率约50%,早期诊断和治疗可改善预后(Chen et al., 2017; Ali-Hasan-Al-Saegh et al., 2023)。非RTAD组3年生存率80%,RTAD组仅60%(Yammine H等研究)。
危险因素
RTAD的病因虽然已被广泛研究,但至今尚未定论。研究表明RTAD可能与操作、支架、主动脉潜在疾病过程本身、弓部解剖以及夹层的自然进展有关。
1. 患者相关因素
一个重要因素是需要TEVAR治疗的患者主动脉潜在疾病过程本身。接受TBAD治疗的患者更容易发生RTAD,即使治疗锚定在“看似健康”的主动脉。最有可能的原因是,炎症和疾病过程超出了主动脉的可见病变段。
主动脉病变类型:夹层,尤其急性患者发生RTAD风险显著高于动脉瘤(相对危险度5.33);急性夹层患者风险是慢性夹层的1.81倍。(Ali-Hasan-Al-Saegh等,2023年)
遗传性胸主动脉疾病:马凡综合征患者风险显著增高,部分研究显示发生率高达25% (Eggebercht等报道48例行TEVAR的马凡患者中RTAD的发生率为8.3%,Dong等报道4例行TEVAR的马凡患者中,3例术后出现RTAD)。
升主动脉直径:直径>40mm(RTAD组47% vs. 非RTAD组21%)。 YammineH等,2019年)
高血压:未控制的高血压会增加RTAD的风险。
2. 操作与器械因素
锚定区位置:1)锚定区靠近Z2区会增加RTAD的风险,最有可能是由于弹性升主动脉和刚性支架移植物之间的不匹配。2)锚定区靠近Z0区或Z1区发生RTAD风险更高)。在一项跨大洲的数据库中,58例全弓去分支0区支架病人中RTAD的发生率高达7.5%。最近一项系统回顾报道3211例TEVAR病人术后RTAD的发生率为2.27%,而0区锚定的病人术后RTAD发生率为6.85。可能与支架回弹力和升主动脉运动相关(Yammine et al., 2019年,Al-Rstum and Afifi,2024年)
支架设计:近端裸支架(PBS)与RTAD更高的发生率无关,而使用连接杆结构且长度<165mm支架会增加TEVAR后RTAD和远端SINE的风险。(Ma et al., 2018年)。
支架尺寸:oversize>20%显著增加主动脉壁上的径向力,导致夹层(Canaud等曾指出,支架oversize>9%会导致RTAD风险增加,每增加一个百分点,风险增加1.4倍)。
技术操作:球囊扩张、导丝/导管操作不当可能导致主动脉壁损伤,增加RTAD风险、经验丰富的中心RTAD发生率较低。 (Yanqing Chen等,2017年)。
3. 术后因素
假腔内漏:假腔中持续的血流增加了RTAD风险。
假腔血栓化:RTAD组假腔血栓化比例更高,可能与血流动力学改变相关(Yammine et al., 2019年)。
血压控制不佳:增加主动脉壁剪切应力(Al-Rstum & Afifi, 2024年)。


治疗与预后
1. 外科手术:
病例分析显示多数RTAD患者需要转心外科行全弓置换术,术后生存率较高。
首选方案:全弓置换+冷冻象鼻术(FET),术后1年生存率90%(Dun et al., 2019)。
急诊手术死亡率:13.6%(30天内),但幸存者长期预后良好(Yammine et al., 2019)。
2. 腔内修复:
在某些情况下,可以考虑再次TEVAR,但在Z0区再次TEVAR可能增加RTAD风险。
预防措施
为尽量减少RTAD的发生率并改善其预后,必须了解其发生的危险因素加以避免,且熟悉RTAD处理的最佳方法。
患者选择
正确的患者评估和方法选择至关重要,包括对潜在疾病的彻底评估,如遗传性胸主动脉疾病、马凡综合征、二叶主动脉瓣或主动脉直径>40 mm。在复杂的TBAD中,TEVAR可能是这一高危人群的救命选择,可能不可避免,因此,意识到可能发生的并发症至关重要!此类人群手术结束时使用成像技术,如血管内超声心动图,有助于早期诊断和治疗RTAD。
杜克大学的一份报告显示,66%的RTAD发生在手术中,75%最初是通过经食管超声心动图或血管内超声发现的,这强调了快速诊断的至关重要性以及术中诊断工具在早期RTAD检测中的潜在作用。
手术优化
选择合适的支架至关重要:避免短支架(<165mm);建议选择径向支撑力小、顺应性好的支架;推荐覆膜支架;oversize控制在10%以内 。
锚定区:优先选择远端锚定区(Z3-Z4),减少弓部机械应力。
操作规范:经验丰富的中心;尽量避免导丝导管损伤、避免球囊扩张(尤其急性夹层)。
术后管理
术后护理和监测在预防RTAD中起着重要作用。
1.严格控制血压(目标<120/80mmHg),戒烟。
2.定期随访(至少每年CTA)。鉴于术后不同时间段可能发生RTAD,TEVAR术后定期随访至关重要。对于高风险人群建议强制必须术后1个月,3个月按时随访。
对患者进行潜在症状教育,如术后胸痛,立即返回医院就医并检查,可及时发现是否有逆撕症状。
(Al-Rstum and Afifi,2024年)

单中心临床病例
我科自2013年12月30日至2023年12月30日行主动脉B型夹TEVAR术632例,RTAD确诊11例(男10例,女1例,年龄39-64;平均年龄53岁),术后早期死亡、高度怀疑RTAD 2例,RTAD占同期主动脉B型夹TEVAR的2.0%。其中死亡5例、失访一例;转心外科行全弓置换+支架象鼻7例,7例痊愈;腔内修复一例,痊愈;总死亡率38.4%。
★ 文献一

Y. Dun et al. Interactive CardioVascular and Thoracic Surgery 2019;
1. 目的
回顾我中心TEVAR后逆行A型主动脉夹层的手术治疗情况。
2. 方法
2014年1月至2018年4月,我中心对22例TEVAR后RTAD患者进行了手术治疗。平均手术年龄52.0±8.0岁。TEVAR和RTAD之间的中位间隔为4.6个月(范围0-120个月)。计算术后死亡率和并发症以评估早期和长期结果。
3. 结果
20例患者行全弓置换术冷冻象鼻技术,2例患者单独行全弓置换术。平均体外循环时间、主动脉阻断时间和选择性脑灌注时间分别为172.4±39.3、100.1±30.3和19.7±10.5min。主要不良事件的发生率为18.6%(4/22),包括1例患者中风,1例患者心肌功能障碍,3例患者肾功能衰竭需要透析。30天内死亡13.6%(3/22例)。所有19名幸存者都有随访数据。平均随访时间为32.2±16.2个月(范围为10-62个月)。随访期间未发生死亡或主动脉相关事件。
4. 结论
伴或不伴有支架象鼻技术的全弓置换术适用于TEVAR后RTAD的治疗,具有可接受的早期和长期效果。
★ 文献二

Fang et al.Frontiers in Cardiovascular Medicine 2022;
1. 目的
本研究目的是描述TEVAR后TAAD的两种不同手术方法,评估其长期预后。
2. 方法
在2010年1月至2019年10月期间,50名之前接受过TBAD TEVAR治疗的患者再次接受了A型主动脉夹层修复。根据患者的CT血管造影和术中发现,我们确定了两组:逆行组(支架诱导的新主动脉损伤,逆行延伸涉及升主动脉)和顺行组(入口撕裂位于主动脉根、升主动脉或主动脉弓,远离支架移植物的边缘)。治疗近端主动脉选择Bentall手术(12/50,24.0%)和升主动脉置换术(38/50,76.0%)。所有患者都接受了全弓置换术(TAR)和冷冻象鼻(FET)植入术。随访期间的生存率采用Kaplan–Meier生存曲线和对数秩检验进行评估。
3. 结果
从既往TEVAR到再次手术的中位间隔时间为187天(IQR:30.01375.0天)。TEVAR后18.0%的TAAD在诊断时没有任何明显症状,大多数症状在常规随访成像中发现。逆行组的患者比顺行组的患者年轻(44.0±9.4 vs.51.4±10.5岁,P=0.012)。两组的术后并发症或死亡率没有显著差异。平均随访时间为3年。术后一年随访,无晚期死亡或并发症发生。术后1年无症状生存率为90.0%。
4. 结论
TAR+FET技术治疗TEVAR后RTAD是可行、有效的。及时手术的成功率和长期预后满意。
★ 典型病例
▎病例一
男性,44岁,慢性B型夹层。2010年12月行TEVAR术。
2013年5月发现RTAD,未处理。2015年2月死亡。
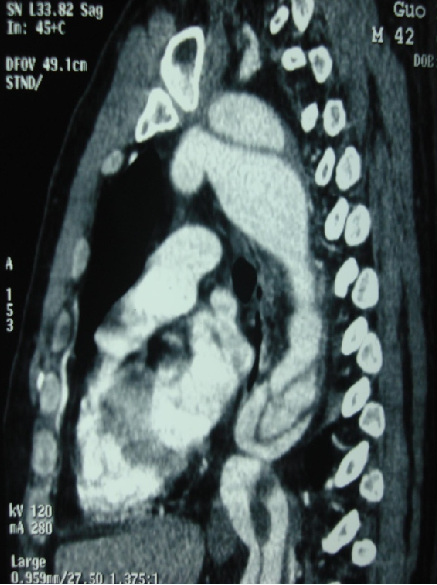
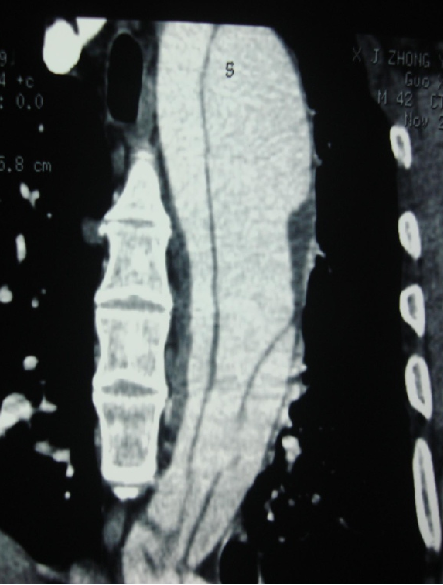
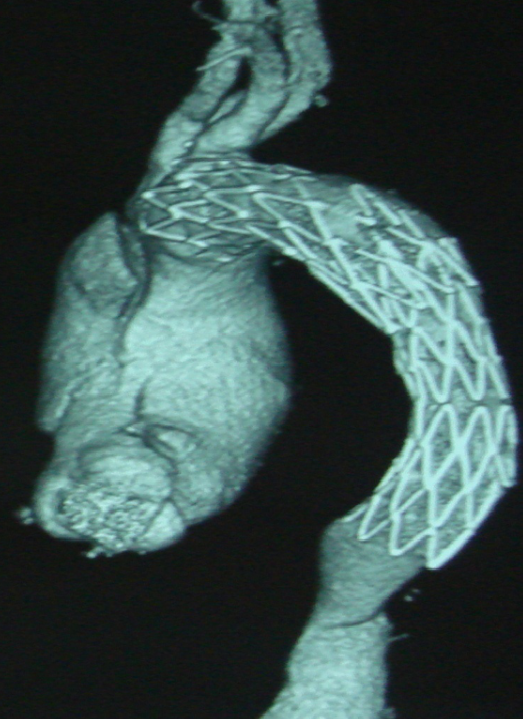
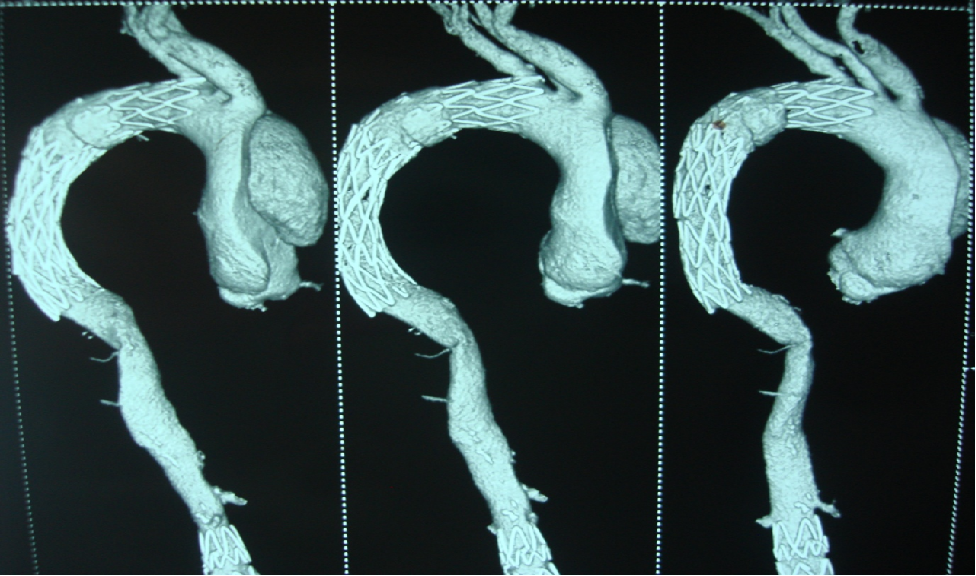
▎病例二
男,52岁,慢性夹层。2015年8月入院,4年前曾因B型层行TEVAR术,主动脉解剖变异,扭曲。行双烟囱+TEVAR术。术后第3天RTAD ,死亡。
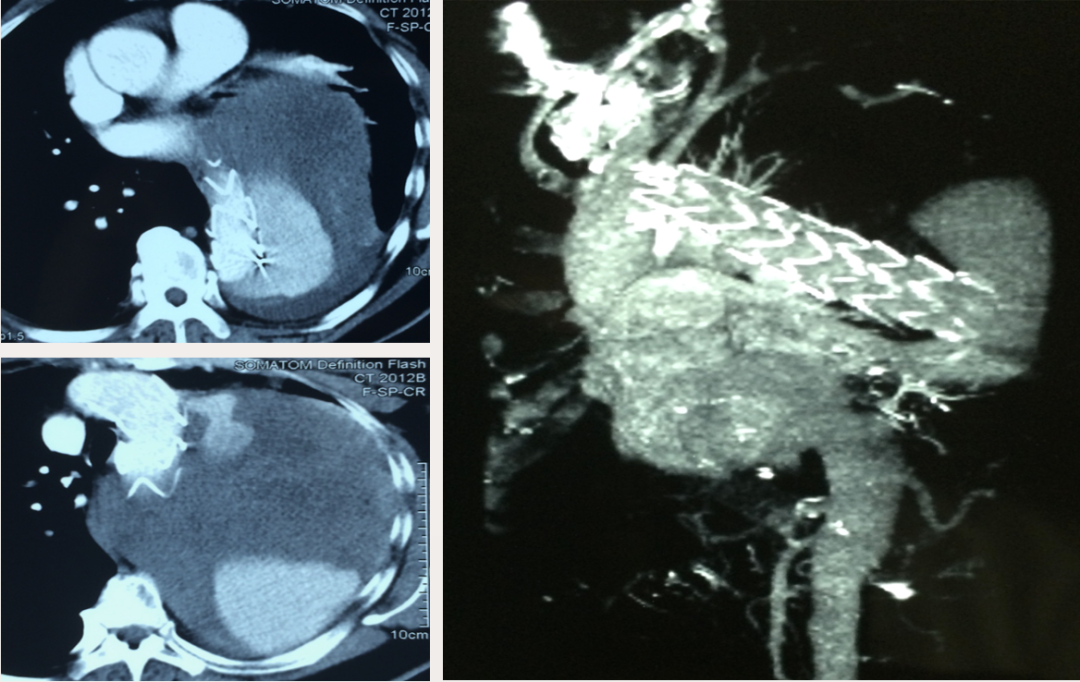
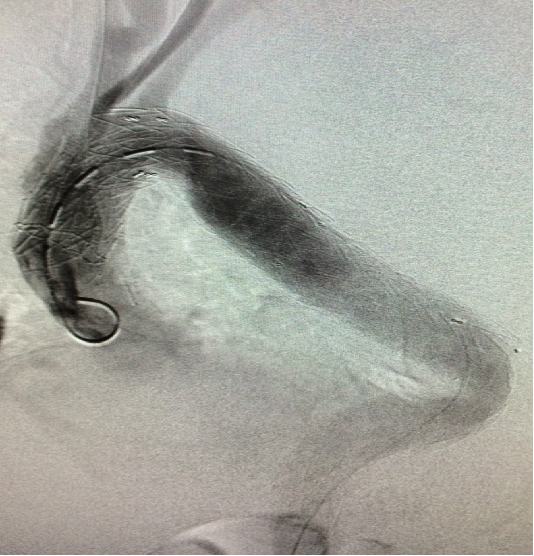
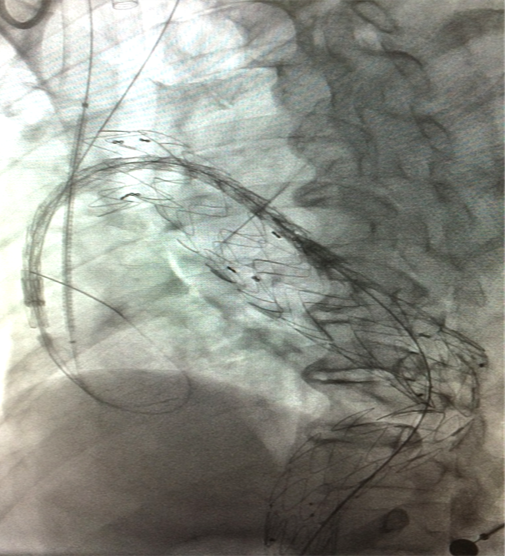
▎病例三
男,60岁,慢性夹层。2013年12月行Debranching+TEVAR术 。2016年7月复查: RTAD ,未手术。失访。
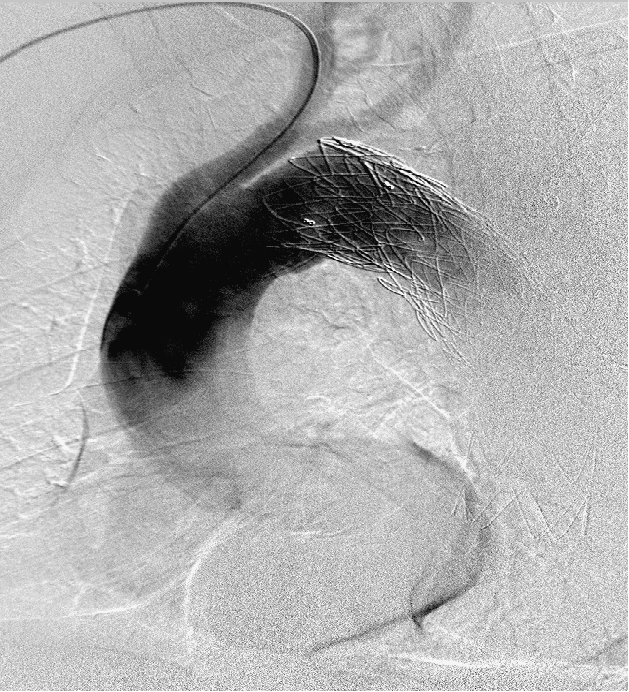
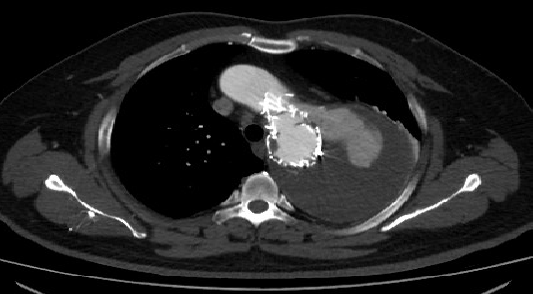
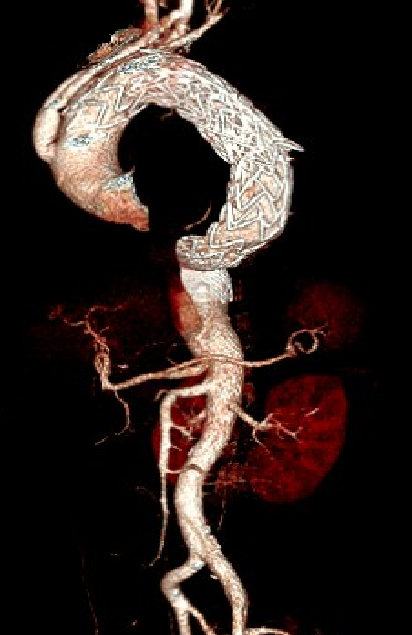
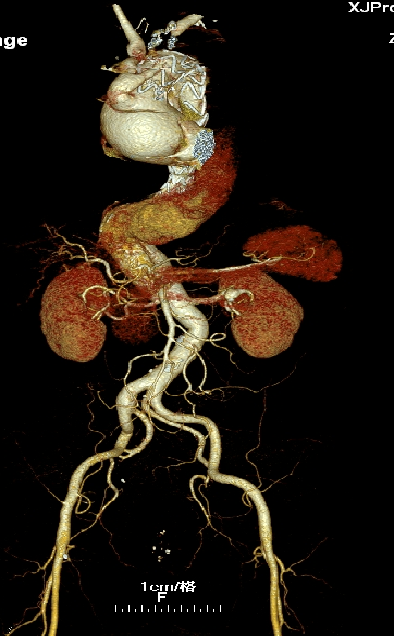
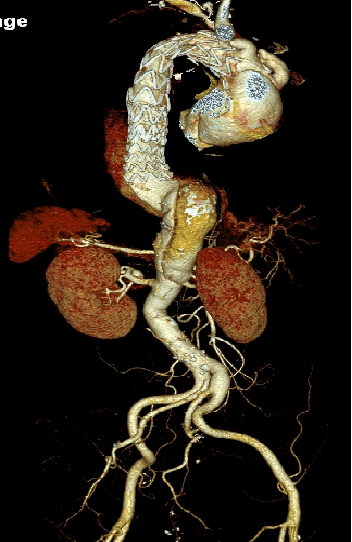
▎病例四
男, 49岁,急性夹层 。2018年11月TEVAR。一月后复查:RTAD 。 2019年1月双开窗。2019年4月2日 复查,结果良好。
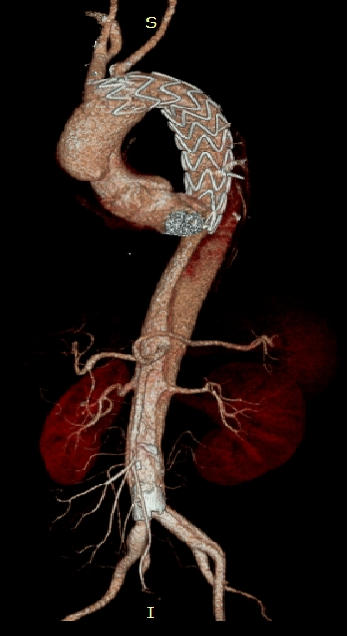
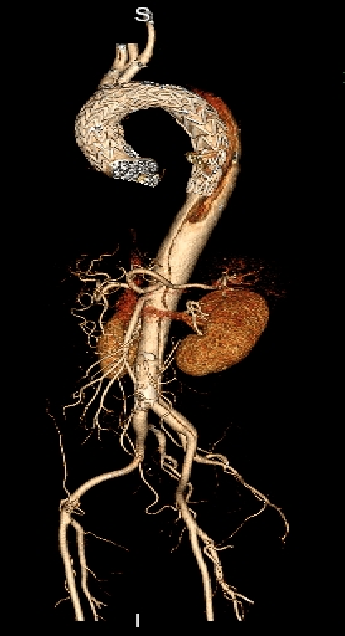
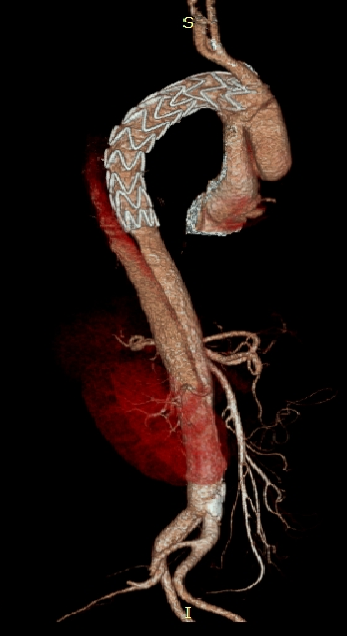
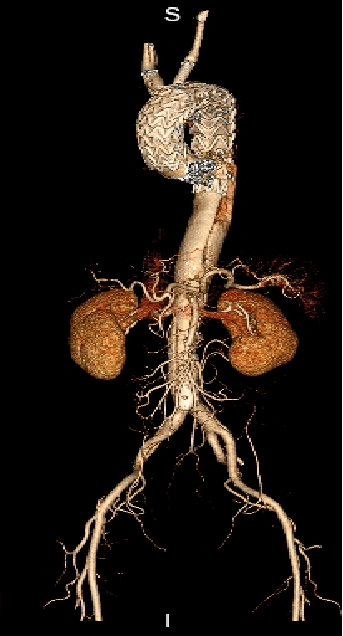
▎病例五
男,49岁,急性AD。2019年1月TEVAR,3月RTAD,行全弓置换+支架象鼻。2022 年1月25日术后复查,结果良好。
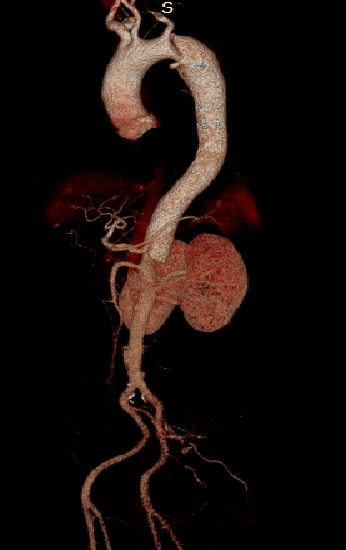
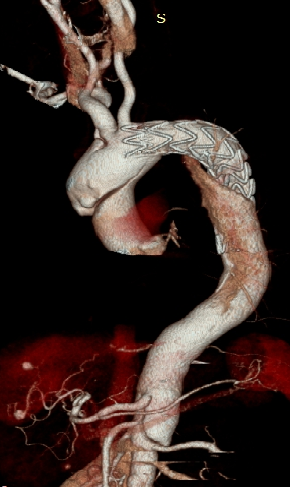
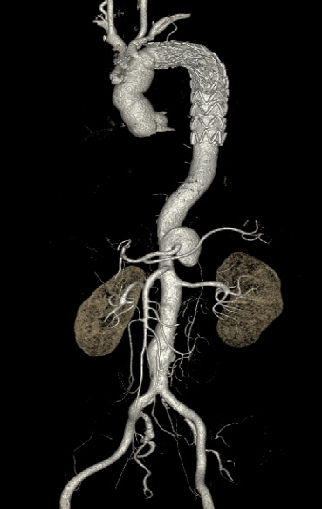
▎病例六
男,50岁,急性夹层。2019年5月TEVAR,术后第4天出院, 意识丧失,死亡。 RTAD ?
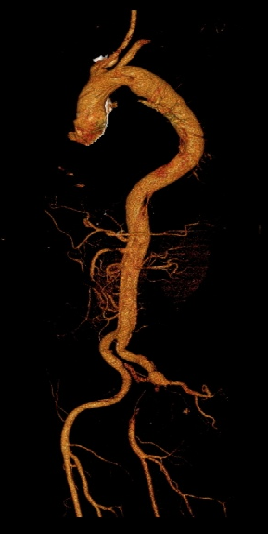
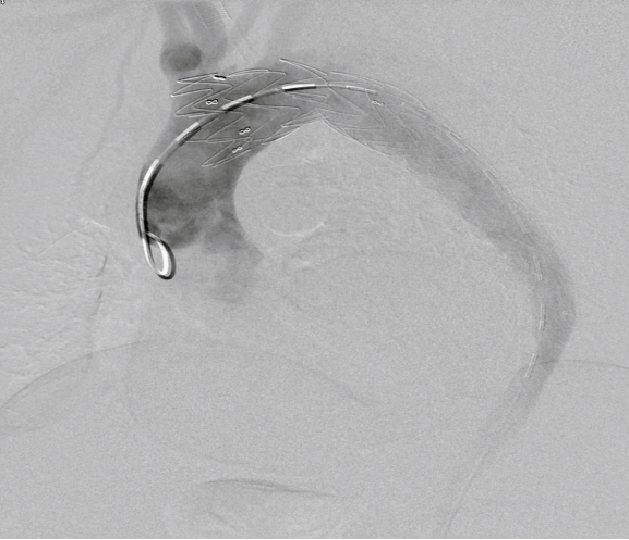
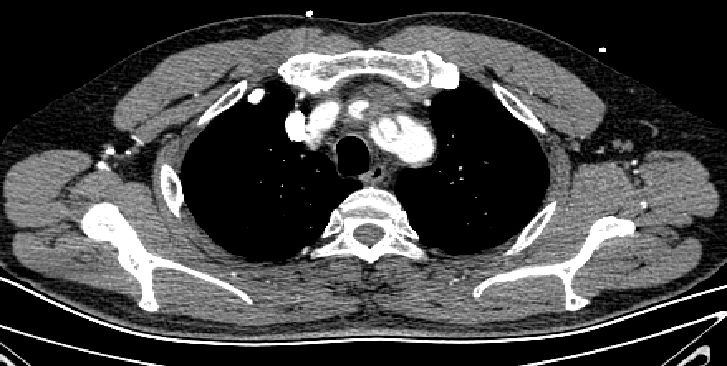
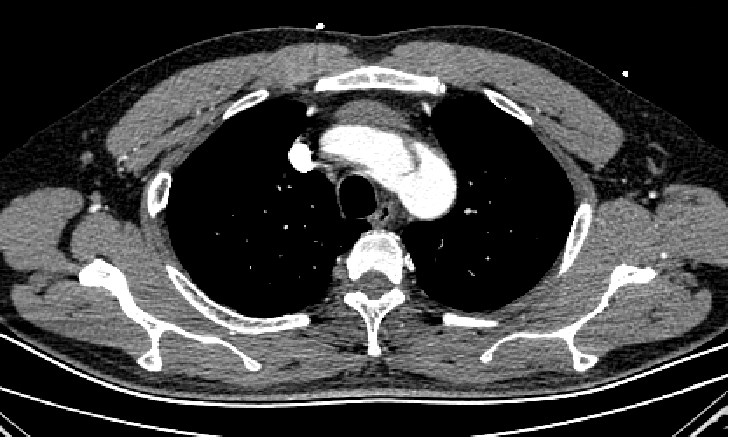
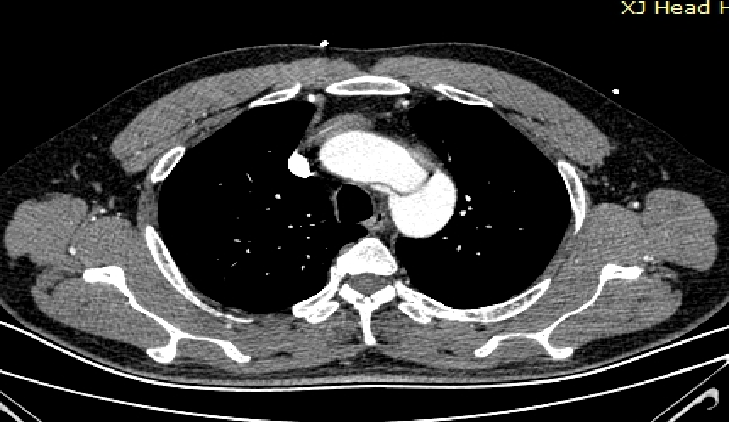
▎病例七
男,54岁,急性夹层。 2023年6月入院,行Debranch+TEVAR。术后出院第四天死亡。 RTAD ?
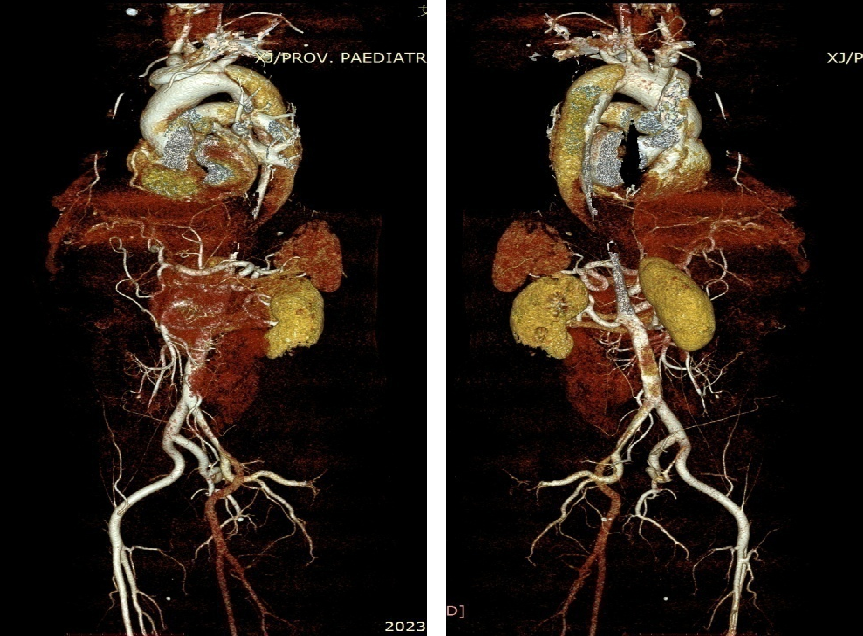
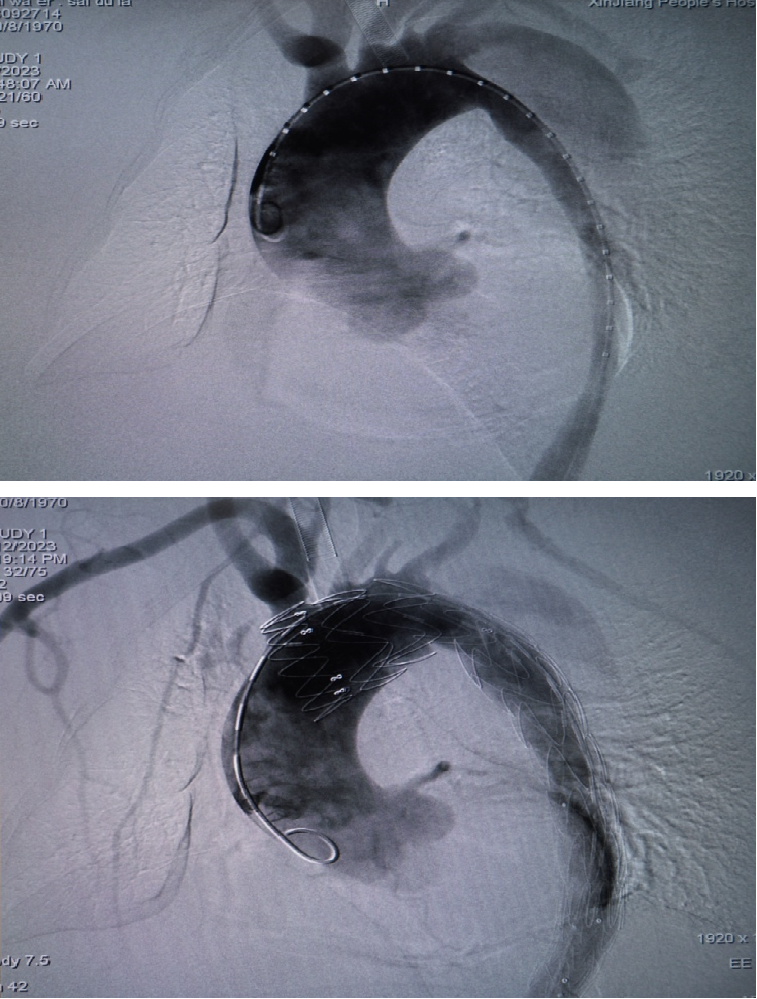
RTAD治疗的“金标准”仍是开放修复。7例RTAD患者转心外科行全弓置换+支架象鼻,7例痊愈。腔内修复在Z0区再次TEVAR很可能再次RTAD。
小结
RTAD是TEVAR术后最严重的并发症之一,发病率低,但死亡率高。
遗传性主动脉病变、支架锚定区在Z0-2区、弓部操作多(开窗、烟囱、debranching)者RTAD风险大。
开放手术仍是RTAD治疗的首选方法,腔内修复在特定情况下可以考虑,但如果发生在Z0区,再次TEVAR很可能再次RTAD。
预防RTAD需要综合考虑患者个体情况和手术技术。术后要特别重视定期随访和症状监测。
专家介绍

戈小虎教授
新疆自治区人民医院
血管外科
主任医师
教授、博士生导师
中国医师协会血管外科医师分会副会长兼血管创伤学组组长
中华医学会外科学分会血管外科学组委员
海峡两岸医药卫生交流协会血管外科学专家委员会副主任委员
国家心血管病专家委员会血管外科专业委员会常委
新疆医学会普外科学专业委员会主任委员
在周围血管外科疾病诊治方面有较深的造诣。主持国家及自治区自然基金等科研项目8项、获得自治区科技进步奖9项,其中一等奖1项,二等奖4项;发表核心期刊及SCI论文60余篇,参与编写专著4部。
