CEC 2025 | 胡海地教授:急性肠系膜缺血的外科治疗


2025年11月6日--9日第十六届中国血管论坛(CEC2025)在北京隆重召开。本次盛会全面展现最新的血管疾病诊疗方法和技术,为广大血管外科医务工作者及同道呈现了一场内容丰富、高质量、高水平的学术盛宴,共话学科发展的崭新未来!欢迎阅读。
演讲题目:
《急性肠系膜缺血的外科治疗》
演讲嘉宾:
胡海地教授
单位:
中国医科大学附属盛京医院

急性肠系膜缺血:血管外科必须掌握的高危急症诊疗策略

它起病隐匿,进展迅猛,死亡率高达60%-80%,甚至超过脑卒中。它被称作“肠卒中”,是血管外科领域公认的急危重症。在临床实践中,我们时常面对辗转多家医院、病情已至晚期的患者,痛惜之余,更需反思:如何提升早期诊断率?如何把握黄金救治时机?开放手术与腔内技术,又该如何协同作战?
本文基于中国医科大学附属盛京医院血管外科胡海地教授的临床经验与深刻洞见,系统梳理急性肠系膜缺血(AMI)的诊疗要点,为奋战在一线的血管外科同道提供一份专业的实战指南。
认识“肠卒中”:一个被严重低估的外科急症
急性肠系膜缺血(Acute Mesenteric Ischemia, AMI)是指肠系膜动脉或静脉因血栓形成、栓塞等原因导致肠管急性血运障碍的疾病。
其临床表现极具迷惑性,尤其是动脉性AMI,早期常表现为剧烈腹痛,但腹部体征轻微,即典型的“症状与体征分离”现象。这一特点极易导致误诊,据统计,初诊误诊率高达50%-60%。
而静脉性AMI则可能起病相对缓慢,直至肠管发生不可逆坏死才出现明显症状。
根据病因不同,其死亡率高达60%-80%。
尽管现代医学已取得长足进步,但AMI的高死亡率依然是悬在我们头顶的达摩克利斯之剑。
病因分型与临床特点:
精准识别是成功的第一步
AMI主要分为三大类型:
动脉阻塞性肠系膜缺血(AOMI):占比最高(60%-70%),其中又以肠系膜上动脉栓塞最为常见(约占67.2%),其罪魁祸首多为心房颤动(房颤)、风湿性心脏病或近期心肌梗死形成的栓子。动脉血栓形成则多发生在动脉硬化基础上。
非阻塞性肠系膜缺血(NOMI):占比约20%-30%,常继发于心力衰竭、休克等导致的全身低灌注状态。
肠系膜静脉血栓形成(MVT):占比10%-15%,其核心病因是高凝状态,包括遗传性易栓症(高同型半胱氨酸血症)、获得性因素(如恶性肿瘤、腹腔炎症、肝硬化、门脉高压)以及大手术后等。
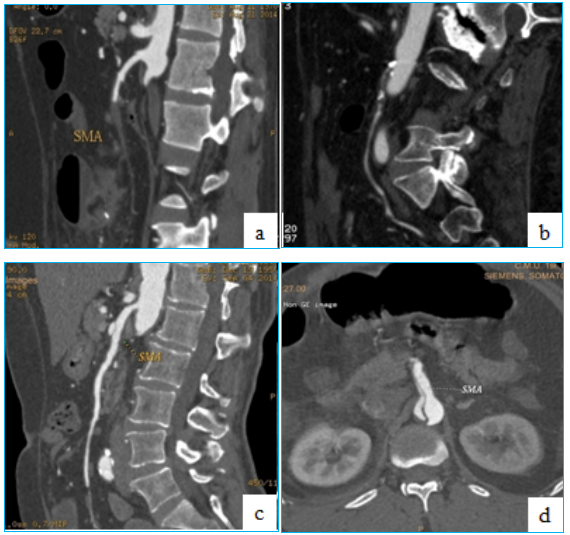
值得注意的是,随着影像学技术的进步,一些过去被忽视的病因,如孤立性肠系膜上动脉夹层、主动脉夹层累及肠系膜血管等,也日益成为AMI的重要原因。
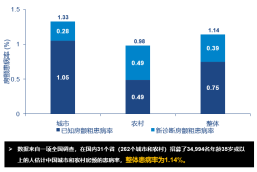
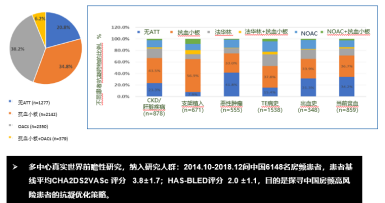
此外,我国房颤患病率已达1.14%,患者基数庞大,但抗凝治疗率却严重不足,大量患者仅依赖阿司匹林,这无疑为AMI的发生埋下了巨大隐患。
诊治路线图:时间就是生命,决策决定成败
Bergan三联征(剧烈腹痛、房颤病史、胃肠道排空症状)和早期“症状体征分离”是重要的预警信号。详细的病史询问(特别是房颤史)和细致的体格检查是基层医生不可忽视的基本功。
面对疑似AMI的患者,必须争分夺秒,建立清晰的诊治思路。胡教授团队的经验为我们提供了一条明确的路径:
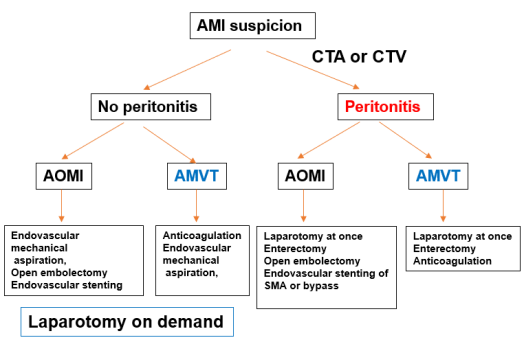
核心原则:有无腹膜炎是决定手术方式的分水岭。
对于已出现腹膜炎体征的患者:无论病因是动脉还是静脉,都意味着肠管很可能已经发生坏死。此时,必须毫不犹豫地选择急诊开腹探查!任何试图先行腔内治疗的犹豫都可能错失挽救生命的最后机会。手术目标明确:切除所有坏死肠管,同时处理血管问题(如动脉取栓,吸栓等)。
对于尚未出现腹膜炎的患者:可优先选择创伤更小的腔内治疗。对于AOMI,可通过导管进行机械吸栓、溶栓或支架置入;对于AMVT,则应立即启动全身抗凝治疗,并密切观察病情变化。若保守或腔内治疗无效,病情恶化出现腹膜炎,则需果断转为开腹手术。
AMVT治疗后应积极避免慢性期改变:门脉海绵样变性→门脉系统静脉高压。
典型案例启示:理论与实践的完美结合
★ 案例一
71岁男性,腹痛2天,房颤患者。
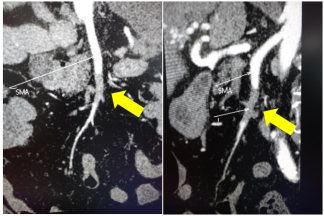
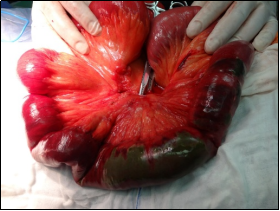
通过开腹取栓+肠切除
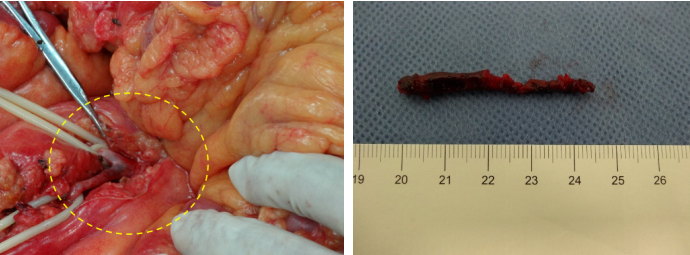
术后恢复良好
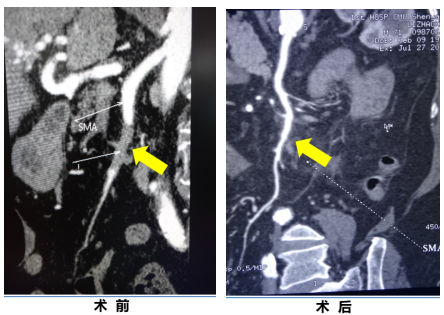
★ 案例二
68岁,男性,突发剧烈腹痛10小时,陈旧性心肌梗死、心房颤动,曾在外院按照急性胆囊炎诊治,因腹痛明显加重来我院急诊。行开腹探查+肠系膜上动脉取栓术。
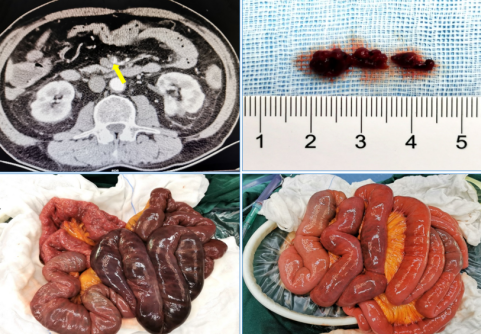
★ 案例三
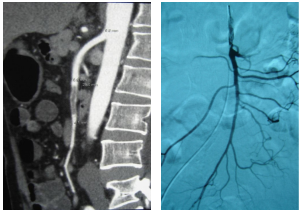
65岁女性,既往心房颤动、脑梗死,20小时前进食后出现剧烈腹痛,并有便血,
CTA示SMA栓塞。在Straub导管吸栓后,利用腹腔镜确认肠管活力,避免了不必要的大切口。这展示了腔内与微创技术结合的可能性。
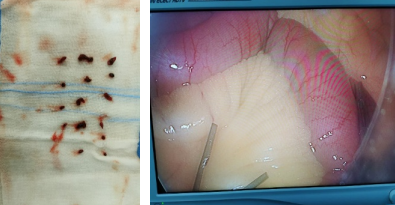
★ 案例四
67岁患者,突发下腹痛2天,既往房颤未系统治疗,全腹增强CT提示肠系膜上动脉血栓、肠梗阻。
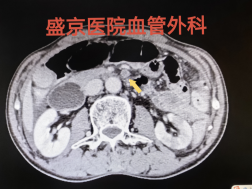
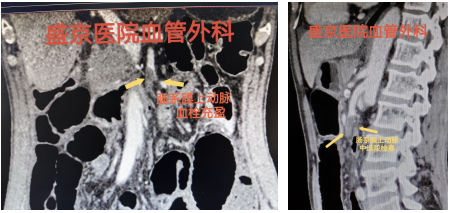
切除后仅剩80cm小肠,通过精心的围手术期管理和长期的家庭肠外营养支持,成功存活。这不仅考验外科技术,更考验整个团队的综合管理能力。
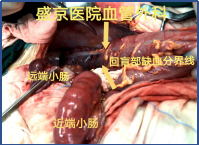
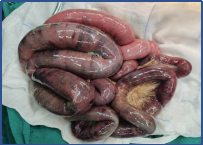
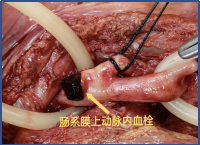
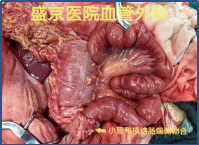
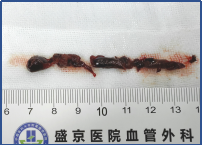
左右滑动查看更多

★ 案例五
全腹持续性腹痛2天;诊断:肠系膜上动脉(分支)闭塞、脾梗死、房颤和弥漫性腹膜炎;查体:全腹压痛、反跳痛伴肌紧张,右侧下腹部腹痛较重;行右半结肠切除术、肠系膜上动脉取栓术,术后经历感染休克关,现患者恢复良好,于血管外科病房治疗中。
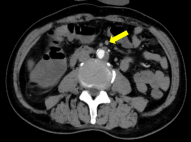
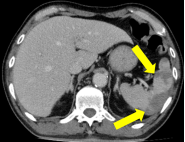
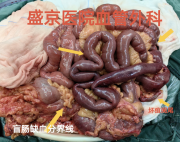
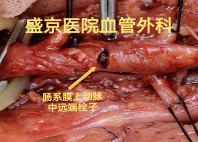
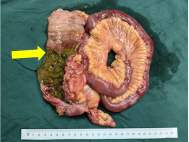
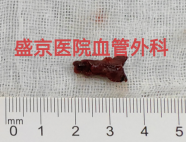
左右滑动查看更多
★ 案例六
25岁,肥胖男性,体重125kg,主诉:腹痛10余天,加重2天、便血1天。
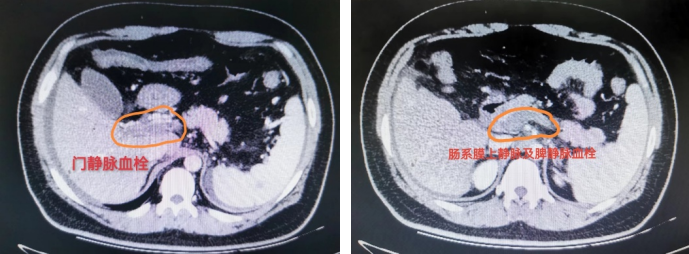
术中及术后标本,术后查因:诊断为高同型半胱氨酸血症 (易栓症),积极术后抗凝、随访中。
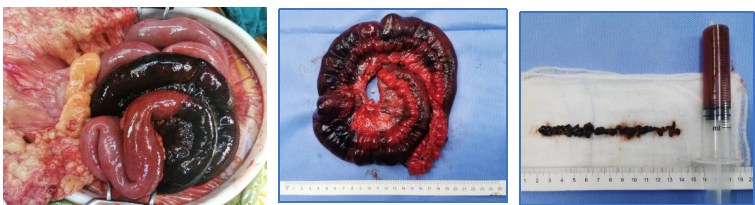
★ 案例七
73岁,德国男性,肥胖体型,既往有糖尿病、冠心病、高血压,主诉:腹痛1周,加重2天。切除坏死小肠380cm,闯过感染休克关、MOF关、切口裂开再手术关、新冠肺炎等关,乘德国医疗转运飞机回国。
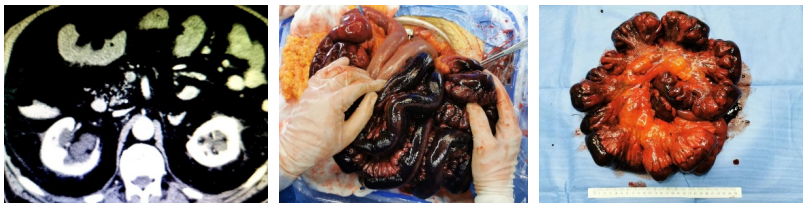
★ 案例八
57岁,女性,主诉:腹痛5天,加重2天,急诊诊断为急性肠系膜静脉血栓形成、急性腹膜炎, WBC30000/ml以上,他院介入科行经皮门静脉肝静脉穿刺吸栓术后,仍然感染性休克。
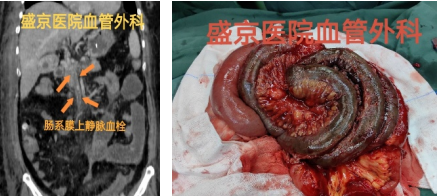
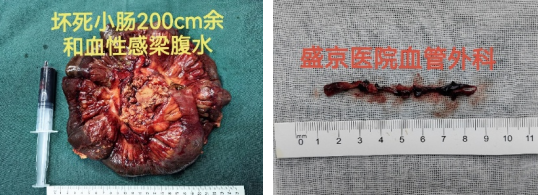
对于急性肠系膜缺血伴有腹膜炎的患者,迅速开腹探查、切除感染坏死肠管是关键!!!
总结与展望:
两手都要硬,方能立于不败之地
AMI的救治是一场与时间的赛跑,更是对血管外科综合实力的全面检验。胡教授在总结中强调了六大关键点:
提高认识,早期诊断、早期干预是改善预后的基石。
腹膜炎是开腹的绝对指征,切勿犹豫。
积极求因,尤其关注易栓症,实现精准治疗。
术后长期、规范的抗凝治疗是防止复发的关键。
密切随访,监测肠功能及凝血状态。
开放手术与腔内技术并重,两手都要抓,两手都要硬。
最后,胡教授特别警示:丧失开放手术能力的血管外科,就如同失去了利爪的猛虎。在介入技术日新月异的今天,我们绝不能丢掉血管外科安身立命的根本——扎实的开放手术基本功。

专家简介

胡海地 教授
中国医科大学附属盛京医院血管外科主任,教授、主任医师、博士生导师
中国医师协会血管外科分会第二届全国委员
辽宁省医学会血管外科学分会候任主任委员
欧美同学会医师协会血管外科分会副主任委员
沈阳市医学会心血管外科学分会副主任委员
国际血管联盟(IUA)中国分部腹主动脉疾病专家委员会委员
中国微循环学会周围血管疾病专业委员中青委副主任委员
亚太血管学术联盟中西医血管病专家委员会副主任委员
